Número atual: 20(1) - Março 2020
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Artigo de Revisao
Eficácia e segurança do Lactobacillus reuteri DSM 17938 nas patologias infantis - Revisão sistemática de estudos randomizados e controlados
Systematic review of RCTs: Lactobacillus reuteri DSM 17938 in diseases of childhood
Cristiane Cremiude Ribeiro-Fernandes; Stevin Zung; Luis Fernando Rensi Cunha; Jana de Ameixa Valentim Fonseca
DOI:10.31365/issn.2595-1769.v20i1p2-9
Aché Laboratórios Farmacêuticos S.A, Gerência Médica Científica - GUARULHOS - São Paulo - Brasil
Endereço para correspondência:
Recebido em: 01/11/2019
Aprovado em: 20/05/2020
Instituição: Aché Laboratórios Farmacêuticos S.A, Gerência Médica Científica
Resumo
INTRODUÇÃO: Probióticos são definidos como micro-organismos vivos que, administrados em quantidades adequadas, conferem benefícios à saúde do hospedeiro. O Lactobacillus reuteri DSM 17938 tem sido amplamente estudado, especialmente em crianças.
OBJETIVO: Diante da grande quantidade de publicações que avaliaram essa cepa probiótica, e o interesse na avaliação dos dados de segurança disponíveis nos estudos, considerou-se válida a realização de uma revisão sistemática atual, avaliando os dados referentes a utilização do Lactobacillus reuteri DSM 17938 nessa população.
FONTES DE DADOS: Em março de 2018 foi realizada busca na literatura com objetivo de localizar RCTs ou revisões sistemáticas desses estudos, já publicados e indexados, realizados em crianças de 0 a 18 anos, avaliando a eficácia do Lactobacillus reuteri DSM 17938 administrado por via oral.
SÍNTESE DOS DADOS E CONCLUSÕES: Ficou demonstrado que o L. reuteri DSM 17938 possui evidência científica suficiente para ser recomendado na cólica do lactente e diarreia aguda. Na dor abdominal funcional e intolerância alimentar os dados apontam para um efeito benéfico dessa cepa, sendo necessários mais estudos clínicos nas mesmas afecções e população. Já na diarreia nosocomial, os dados dos artigos, não indicam que haja benefício da cepa quando utilizada em crianças.
Palavras-chave: Lactobacillus reuteri; Criança; Eficácia; Segurança; Revisão.
Abstract
INTRODUCTION: Probiotics are living microorganisms, which when administered in adequate amounts, confer benefits to the health of the host. The strain Lactobacillus reuteri DSM 17938 has been extensively studied, especially in children.
OBJECTIVES: In view of the large amount of publications that evaluates the probiotic strain and the interest in the evaluation of the safety data of the studies, the existence of a current systemic revision was considered, evaluating the data regarding the use of Lactobacillus. reuteri DSM 17938 in this population.
DATA SOURCE: In March 2018 it was conducted a search on literature with the objective to detect randomized controlled trials or systematic reviews of these already published and indexed studies conducted in children aged 0 to 18 years, evaluating the efficacy of orally Lactobacillus reuteri DSM 17938.
DATA SYNTHESIS AND CONCLUSIONS: It has been demonstrated that Lactobacillus reuteri DSM 17938 has sufficient scientific evidence to be recommended in infant colic and acute diarrhea. In functional abdominal pain and food intolerance, the data point to a beneficial effect of this strain, requiring more clinical studies in the same conditions and population. In nosocomial diarrhea data from the articles, do not indicate that there is benefit of the strain when used in children.
Keywords: Lactobacillus reuteri; Child. Efficacy; Safety; Systematic Review.
INTRODUÇÃO
Há mais de um século, Elie Metchnikoff, pesquisador russo e ganhador do Nobel, postulou que "bactérias ácido láticas" ofereceriam benefícios a saúde capazes de promover longevidade1. Já há vários anos utiliza-se o conceito de probióticos, micro-organismos vivos que, administrados em quantidades adequadas, conferem benefícios à saúde do hospedeiro2,3.
Dentre os diferentes mecanismos de ação apresentados para os probióticos, destacam-se sua atividade como primeira linha de defesa para repelir micro-organismos patogênicos no trato gastrointestinal e contribuição para a imunidade específica contra patógenos4.
Bifidobacteria e Lactobacillus spp. são os gêneros mais utilizados como probióticos e os de origem humana mais eficazes5. Um representante do segundo é o Lactobacillus reuteri (L. reuteri), bactéria gram-positiva isolada do leite humano ou trato gastrointestinal; várias de suas cepas foram estudadas em diversas patologias e consideradas benéficas6. Evidências atuais indicam que os efeitos probióticos são específicos para cada linhagem ou cepa7. A cepa L. reuteri DSM 17938, obtida através da remoção natural de dois plasmídeos portadores de genes de resistência a antibióticos da cepa mãe L. reuteri ATCC 55730, foi avaliada em múltiplos estudos6,8,9.
Um dos mais bem documentados mecanismos de ação do L. reuteri é a sua atividade antimicrobiana; algumas linhagens, inclusive o DSM 17938, produzem reuterina, substância capaz de inibir o crescimento de ampla gama de micro-organismos potencialmente patogênicos. Algumas linhagens de L. reuteri também podem regular as respostas imunológicas10.
A segurança dos produtos contendo probióticos tem sido alvo de estudos, especialmente diante da disseminação de sua utilização em diversos cenários, com preocupação especialmente relacionada aos riscos de bacteremia e/ou fungemia11.
Em 2014 foi publicada revisão sistemática avaliando a eficácia do L. reuteri DSM 17938 na população pediátrica10. Diante da grande quantidade de publicações que avaliaram a mesma cepa posteriormente, e do interesse na avaliação de dados de segurança apresentados, considerou-se válida a realização de nova revisão sistemática, baseada em estudos clínicos randomizados e controlados (RCTs) ou revisões sistemáticas desses.
MÉTODOS
Foi conduzida revisão sistemática utilizando como base a ferramenta PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-analysis)12. Em março de 2018 realizou-se busca na literatura para localizar RCTs ou revisões sistemáticas, englobando crianças menores 18 anos, avaliando a eficácia da administração oral do Lactobacillus reuteri DSM 17938. As buscas foram realizadas nas bases de dados PubMed e SciELO. Na PubMed foram utilizadas as estratégias de busca"lactobacillus reuteri DSM 17938"; "lactobacillus reuteri AND DSM17938"; "L. reuteri AND DSM 17938"; "L. reuteri AND DSM17938"; "lactobacillus AND protectis"; "lactobacillus AND prodentis". Foram localizados 214 resultados. Na base SciELO foi utilizada a estratégia de busca "lactobacillus reuteri" que resultou em 23 estudos. Adicionalmente, foram incluídos consensos e diretrizes relacionados aos tópicos abordados. Utilizou-se a ferramenta da Cochrane Collaboration para avaliação do risco de viés dos estudos. Já para as revisões sistemáticas, foi utilizada a ferramenta AMSTAR. Um pesquisador realizou toda a avaliação dos resultados obtidos, que foram validados por um segundo investigador. O protocolo desta revisão sistemática foi registrado na base International Prospective Register of Systematic Reviews (PROSPERO - Registro CRD42018108949). Como os trabalhos escolhidos são bastante heterogêneos, não foram realizadas análises estatísticas adicionais como de risco relativo ou diferença média.
RESULTADOS
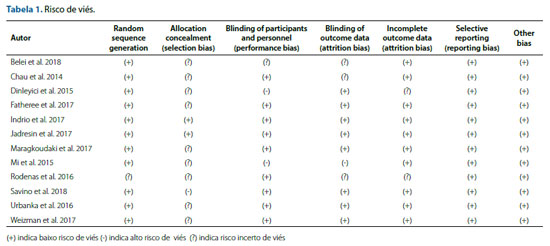
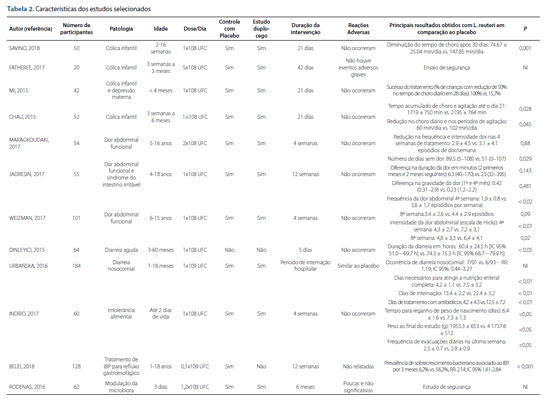
Foram selecionados 12 RCTs, cujos desfechos clínicos foram considerados relevantes, além de 5 revisões sistemáticas de RCTs. Na Figura 1 está detalhado o motivo de exclusão dos 220 estudos. Os artigos, em inglês, foram publicados a partir do ano de 2014 e avaliaram a cepa Lactobacillus reuteri DSM 17938. Tal data foi selecionada pois houve a publicação de revisão sistemática de escopo similar. As idades dos participantes variaram de dois dias a 18 anos. A Tabela 1 apresenta o risco de viés de cada um dos RCTs selecionados; em geral o risco apresentado foi baixo. A Tabela 2 sumariza informações dos RCTs. As revisões sistemáticas apresentadas foram classificadas com AMSTAR entre 5 a 9 - de 11 pontos atribuíveis.
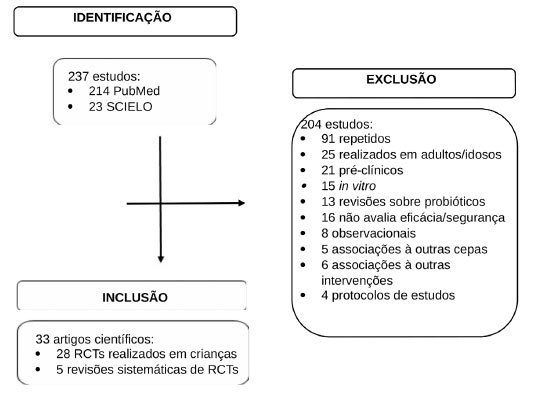
Figura 1. Fluxograma de estudos incluídos na revisão sistemática.
A seguir, serão descritos, de forma sumarizada, os principais resultados clínicos encontrados nos estudos científicos selecionados. Os trabalhos foram agrupados em diferentes afecções em que houve a utilização do L. reuteri, sendo elas: cólica no lactente, dor abdominal funcional, diarreia aguda, diarreia nosocomial, intolerância alimentar e modulação da microbiota.
Cólica no lactente
Um RCT duplo-cego avaliou 60 bebês com cólica recebendo L. reuteri (1x108 UFC/dia) ou placebo durante 1 mês. No 30º dia, o tempo de choro foi menor entre os lactentes com cólica no grupo probiótico em comparação ao placebo (79 minutos versus 135 minutos - p = 0,001). O probiótico aumentou a porcentagem de Lactobacillus (p = 0,049) e diminuiu a calprotectina fecal (p = 0,0001). Não foram reportados eventos adversos13.
Foi realizado um ensaio de segurança, em 20 crianças com cólica, amamentadas, de 3 semanas a 3 meses, que receberam L. reuteri (5x108 UFC) ou placebo durante 42 dias e seguidos por 134 dias. Dentre esses, 55% apresentaram contagens baixas de neutrófilos (<1500/mm3), que se normalizaram em todos os bebês no dia 176. O probiótico não produziu eventos adversos graves e não alterou significativamente o tempo de choro, o bicarbonato plasmático ou os biomarcadores inflamatórios. A calprotectina fecal diminuiu rapidamente em ambos os grupos. Nos lactentes com gram-negativos fecais dominantes, a resolução da cólica foi associada a reduções acentuadas nesses organismos14.
Em estudo simples-cego avaliou-se o uso de L. reuteri na dose de 1x108 UFC (n = 21) ou placebo (n = 21) na cólica em crianças menores de 4 meses durante 21 dias. Houve redução no tempo médio diário de choro em 100% do grupo probiótico, e em 15,7% do grupo placebo (p < 0,01). Tal redução foi significativa mesmo durante a 1ª semana (p < 0,01). A satisfação dos pais e a melhora na depressão materna foi significativamente maior no grupo probiótico. Não se relataram eventos adversos15.
Um estudo duplo-cego avaliou a eficácia do Lactobacillus reuteri (1x108 UFC - n = 24) na cólica em 52 lactentes, comparado ao placebo (n = 28), administrados durante 21 dias. O tempo médio de choro e agitação foi menor no grupo probiótico (p = 0,028). O probiótico promoveu redução no choro diário e nos períodos de agitação no final do período de tratamento (p = 0,045). No dia 21, uma proporção maior de bebês do grupo L. reuteri respondeu ao tratamento com redução do tempo de choro ≥ 50% em comparação ao placebo (p = 0,035). Nenhum evento adverso foi relatado3.
A revisão anteriormente conduzida concluiu, embasada nas publicações anteriores a 2014, que a cepa provavelmente reduz o tempo de choro na cólica do lactente. De acordo com dados do ROMA IV, existem evidências de que a suplementação com probióticos, como o L. reuteri, pode reduzir o choro. No mesmo documento, cita-se apenas um estudo no qual não foi observado benefício com a utilização do probiótico16. Revisão sistemática publicada em 2015 concluiu que essa cepa apresentou eficácia na cólica infantil com redução no tempo de choro em 2 a 3 semanas17. Em uma meta-análise publicada em 2017 o L. reuteri e algumas abordagens dietéticas superaram outras intervenções na cólica infantil, com aparente superioridade do primeiro18. Em outra meta-análise, publicada por Sung e cols., afirmou- se que o probiótico foi eficaz e pode ser recomendado para bebês com cólica amamentados19.
DOR ABDOMINAL FUNCIONAL (DAF)
Um RCT avaliou 54 crianças (9.1 ± 3,8 anos) com DAF que receberam 2x108 UFC de L. reuteri (n = 27) ou placebo (n = 27) durante 4 semanas. Ambos reduziram significativamente a frequência e a intensidade dos episódios de dor abdominal na 4ª e 8ª semanas (p < 0,001). Apenas no grupo probiótico diminuiuse o uso de medicamentos para alívio da dor na 4ª semana, e o número de faltas à escola e ausências no trabalho, na 4ª e 8ª semanas. Não se atingiu significância estatística. Nenhuma reação adversa foi registrada20.
O segundo RCT avaliou o efeito dessa cepa, na dosagem diária de 1x108UFC, no tratamento da DAF ou síndrome do intestino irritável em 55 crianças entre 4-18 anos, (26 = intervenção e 29 = placebo). No grupo intervenção houve mais dias sem dor (p = 0,029), e a dor abdominal foi menos grave no 2º (p < 0,05) e no 4º mês (p <0,01). Todos os participantes apresentaram redução na gravidade da dor abdominal do 1º ao 4º mês, com redução mais proeminente no grupo intervenção (p < 0,001 versus p = 0,004). Não foram relatados eventos adversos21.
Em um outro RCT, 101 crianças de 6 a 15 anos receberam L. reuteri ou placebo durante 4 semanas. O probiótico (n = 47) foi superior ao placebo (n = 46) na redução da frequência (1,9 versus 3,6 episódios por semana, respectivamente - p < 0,02) e intensidade (4,3 versus 7,2 na escala de Hicks, respectivamente - p < 0,01) da dor abdominal após 4 semanas. Em 8 semanas, o L. reuteri foi superior na melhora da intensidade da dor abdominal (4,8 versus 4,1). Houve uma menor incidência de distensão abdominal e inchaço, favorecendo o grupo probiótico. Não houve efeitos significantes nos demais desfechos ou relato de eventos adversos22.
Revisão de 2014 concluiu que evidencia limitada sugeria potencial utilidade dessa cepa na DAF. Embora a administração deste probiótico pareça ser associada à possível redução da intensidade da dor e mais dias sem dor em pacientes com DAF, tal entendimento ainda não foi considerado no ROMA IV16.
Diarreia aguda
Um RCT, simples-cego, avaliou o L. reuteri (1x108 UFC), durante 5 dias, em associação a solução de reidratação oral, comparado a reidratação isolada, em 64 crianças com diarreia infecciosa ambulatorial. Houve redução na duração média do sintoma em 33 horas (p < 0,05) e menor quantidade de crianças com diarreia (44,8% versus 87%) (p < 0,01) no grupo L. reuteri em comparação ao grupo controle. Não foram observados efeitos adversos23.
Em revisão de 2014, considerou-se que os dados documentavam a eficácia da cepa. Tais resultados são corroborados pela European Society for Pediatric Gastroenterology, Hepatology, and Nutrition (ESPGHAN) e European Society of Pediatric Infectious Diseases (ESPID), que incluíram o L. reuteri DSM 17938 na lista de cepas recomendadas na diarreia aguda24. Adicionalmente, em revisão sistemática de 2016, demonstrou-se que a administração dessa cepa reduziu a duração da diarreia e aumentou a chance de cura. Como prevenção, o L. reuteri apresentou potencial de reduzir o risco de diarreia adquirida na comunidade25.
Diarreia nosocomial
Um RCT duplo-cego avaliou a eficácia do probiótico (1x109 UFC/dia) na prevenção de diarreia nosocomial. Participaram do estudo 184 crianças (1-48 meses) internadas no hospital por outras razões que não diarreia. Foi administrado L. reuteri (n = 91) ou placebo (n = 93). A diarreia nosocomial ocorreu em 7,1%. Nenhuma diferença foi encontrada na prevenção da diarreia e em outros desfechos, incluindo eventos adversos26.
Na revisão anterior, concluiu-se que não havia evidência da efetividade dessa cepa na prevenção de diarreia nosocomial. De acordo com dados do ESPGHAN/ESPID, para a diarreia nosocomial geralmente não são necessários medicamentos; entretanto, probióticos selecionados podem reduzir a duração e a intensidade dos sintomas27.
Intolerância alimentar
Estudo clínico duplo-cego avaliou o L. reuteri (1x108 UFC) em 60 bebês prematuros randomizados durante as primeiras 48 horas de vida para receber L. reuteri ou placebo durante 1 mês. O probiótico promoveu diminuição no número de dias até atingir a nutrição enteral completa (p < 0,01), de internação (p < 0,01) e de tratamento com antibióticos (p < 0,01). L. reuteri aumentou a citocina anti- inflamatória interleucina (IL)-10. Já dentre as citocinas pró-inflamatórias, os níveis de IL-17, IL-8 e fator de necrose tumoral alfa foram aumentados no grupo placebo. Não houve relatos de eventos adversos. Trata-se de estudo único que, embora insuficiente para compor uma recomendação, demonstra a necessidade de novos estudos para a avaliação do papel dessa cepa no manejo da intolerância alimentar28.
Modulação da microbiota
Foi realizado RCT avaliando a prevalência de sobrecrescimento bacteriano no intestino delgado em 128 crianças (1-18 anos) com Doença do Refluxo Gastroesofágico (DRGE) que receberam 12 semanas de inibidor de bomba de prótons (IBP) com ou sem L. reuteri (0,1x109 UFC) associado, em comparação a grupo controle (120 crianças hígidas). As crianças com DRGE em uso de IBP foram randomizadas: placebo (n = 64) e probiótico (n = 64). Ao final do tratamento houve disbiose em 56,2% do grupo placebo (36/64), e em 6,2% do grupo probiótico (p < 0,001). O grupo que recebeu probiótico apresentou menor prevalência de disbiose, semelhante ao controle (p = 0,740). Não há informações sobre eventos adversos29.
Um RCT duplo-cego avaliou 62 bebês nascidos de parto cesárea (PC) ou parto vaginal (PV) que receberam fórmula (F) ou fórmula + L. reuteri (1,2x109 UFC) (FLR), 72 horas após o nascimento até os 6 meses de idade. Os perfis filogenéticos da microbiota dos demais grupos divergiram do grupo PCF na 2ª semana. Não houve alteração importante na microbiota em bebês nascidos de parto vaginal; já no parto cesariana, a cepa pareceu modular o desenvolvimento inicial da microbiota. O número de eventos adversos foi baixo e não significativo30.
De acordo com Diretrizes da Organização Mundial de Gastroenterologia, essa cepa é recomendada como probiótica em diversas afecções gastrointestinais que atuam através do equilíbrio da microbiota1.
DISCUSSÃO
Como nos últimos anos houve aumento considerável de estudos clínicos realizados com a cepa Lacctobacillus reuteri DSM 17938 em diferentes afecções da infância, o objetivo desta revisão foi o de agrupar os dados de RCTs, publicados posteriormente a revisão sistemática de 2014, para determinar se o L. reuteri DSM 17938 poderia ser recomendado em diferentes patologias infantis. Foram utilizadas diferentes estratégias de busca para a seleção de estudos; assim, houve grande número de publicações repetidas (91), retiradas da análise. Não foram encontrados artigos posteriores à data de avaliação considerada na revisão de Urbanska relacionados aos temas prevenção da cólica e regurgitação, constipação, prevenção de infecções e prevenção de enterocolite necrotizante. Quanto aos demais temas, os dados expostos corroboram o trabalho citado, que concluiu que essa cepa pode ser benéfica em diversas afecções da infância, sem demonstrar benefício na diarreia nosocomial. Na cólica do lactente, a cepa mostrou-se benéfica na maior parte dos estudos, especialmente em bebês amamentados. Para aqueles que recebem fórmula exclusivamente ou de forma complementar, seu benefício carece de mais estudos. Na intolerância alimentar e modulação da microbiota, não foi possível realizar comparativo, uma vez que tais desordens não foram avaliadas no trabalho anterior. Os dados agrupados desta revisão indicam que o L. reuteri DSM 17938 pode ser utilizado na cólica do lactente, diarreia aguda e equilíbrio da microbiota intestinal. Houve resultados positivos, mas ainda não apoiados por consensos na dor abdominal funcional. Já na intolerância alimentar ainda não há evidência suficiente para a recomendação desta cepa. Na diarreia nosocomial a cepa não encontra respaldo em literatura. Como a literatura é muito vasta com a cepa supracitada, não foi possível haver um aprofundamento em cada uma das afecções nas quais houve a utilização do L. reuteri, no entanto, foi realizada busca detalhada e apresentação sumarizada de todos os dados de todos os estudos clínicos que atenderam aos critérios de inclusão dessa revisão sistemática. Uma outra limitação deste trabalho é que como os artigos selecionados são bastante heterogêneos, com diferentes patologias, desfechos observados e formas de mensuração destes, não foi possível realizar análise de mensuração de dados em uma metaanálise. Em algumas afecções o pequeno número de estudos ainda não fornece dados conclusivos para recomendar o L. reuteri DSM 17938. A cepa DSM 17938 continua sendo considerada segura. Posteriormente à conclusão da pesquisa realizada para compor essa revisão sistemática, foi publicada uma meta análise avaliando o efeito do L. reuteri DSM 17938 na gastroenterite em crianças, o trabalho concluiu que, embora tenha havido resultado benéfico, o pequeno efeito de relevância clínica e as limitações metodológicas devem ser considerados31.
CONCLUSÕES
Ao avaliar os estudos publicados posteriormente a 2014, essa revisão conclui que o L. reuteri DSM 17938 possui evidência científica para ser recomendado na cólica do lactente3,13,14,15, diarreia aguda23 e equilíbrio da microbiota29,30, uma vez que os trabalhos publicados apresentaram, em sua maioria, benefícios aos bebês ou crianças. Na dor abdominal funcional20,21,22 e intolerância alimentar28, embora haja dados que apontem para sua eficácia, são necessários mais estudos clínicos para o estabelecimento da recomendação. Já na diarreia nosocomial26, os dados localizados nos trabalhos publicados não indicam que haja benefício da cepa nessa população.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Guarner F, Sanders ME, Eliakim R, Fedorak R, Gangl A, Garish J. et al. Probióticos e prebióticos. Diretrizes Mundiais da Organização Mundial de Gastroenterologia. 2017.
2. Senok AC, Ismaeel AY, Botta GA. Probiotics: facts and myths. Clinical Microbiology and Infection.2005;11(12):958-966.
3. Chau K, Lau E, Greenberg S, Jacobson S, Yazdani-Brojeni P, Verma N, Koren G. Probiotics for infantile colic: a randomized, doubleblind, placebo-controlled trial investigating Lactobacillus reuteri DSM 17938. The Journal of pediatrics.2015;166(1):74-78.
4. Garofoli F, Civardi E, Indrio F, Mazzucchelli I, Angelini M, Tinelli C, et al. The early administration of Lactobacillus reuteri DSM 17938 controls regurgitation episodes in full-term breastfed infants. International journal of food sciences and nutrition.2014:65(5), 646-648.
5. Indrio F, Riezzo G, Raimondi F, Bisceglia M, Filannino A, Cavallo L, et al. Lactobacillus reuteri accelerates gastric emptying and improves regurgitation in infants. European journal of clinical investigation.2010;41(4):417-422.
6. Dinleyici EC, PROBAGE Study Group, Vandenplas Y. Lactobacillus reuteri DSM 17938 effectively reduces the duration of acute diarrhoea in hospitalised children. Acta Paediatrica. 2014;103(7):e300-e305.
7. McFarland LV, Evans CT, Goldstein EJ. Strain-specificity and disease-specificity of probiotic efficacy: a systematic review and meta-analysis.2018. Frontiers in medicine;5.
8. Szajewska H, Gyrczuk E, Horvath A. (2013). Lactobacillus reuteri DSM 17938 for the management of infantile colic in breastfed infants: a randomized, double-blind, placebo- controlled trial. The Journal of pediatrics.2013:162(2):257-262.
9. Savino F, Cordisco L, Tarasco V, Palumeri E, Calabrese R, Oggero R et al. Lactobacillus reuteri DSM 17938 in infantile colic: a randomized, double-blind, placebo-controlled trial. Pediatrics.2010:126(3);e526.
10. Urbańska M, Szajewska H. The efficacy of Lactobacillus reuteri DSM 17938 in infants and children: a review of the current evidence. European journal of pediatrics. (2014);173(10):1327- 1337.
11. Didari T, Solki S, Mozaffari S, Nikfar S, Abdollahi M. (2014). A systematic review of the safety of probiotics. Expert opinion on drug safety.2014;13(2):227-239.
12. Hutton B, Salanti G, Caldwell DM, Chaimani A, Schmid CH, Cameron C, et al. The PRISMA extension statement for reporting of systematic reviews incorporating network meta- analyses of health care interventions: checklist and explanations. Annals of internal medicine.2015;162(11):777-784.
13. Savino F, Garro M., Montanari P, Galliano I, Bergallo M. Crying Time and RORγ/FOXP3 Expression in Lactobacillus reuteri DSM17938-Treated Infants with Colic: A Randomized Trial. The Journal of pediatrics.2018;192:171-177.
14. Fatheree NY, Liu Y, Taylor CM, Hoang TK, Cai C, Rahbar MH, et al. Lactobacillus reuteri for infants with colic: a double-blind, placebo-controlled, randomized clinical trial. The Journal of pediatrics.2017:191:170-178.
15. Mi GL, Zhao L, Qiao DD, Kang WQ, Tang MQ, Xu JK. Effectiveness of Lactobacillus reuteri in infantile colic and colicky induced maternal depression: a prospective single blind randomized trial. Antonie Van Leeuwenhoek.2015;107(6):1547-1553.
16. Drossman DA, Chang L, Chey WD, Kellow J, Tack J, Whitehead WE, et al. ROME IV - Functional Gastrointestinal Disorders - Disorders of Gut-Brain Interaction. Volume II, 4th edition. NC: Springer Healthcare: 2016.
17. Xu M, Wang J, Wang N, Sun F, Wang L, Liu XH. The efficacy and safety of the probiotic bacterium Lactobacillus reuteri DSM 17938 for infantile colic: a meta-analysis of randomized controlled trials. PloS one.2015;10(10):e0141445.
18. Gutiérrez-Castrellón P, Indrio F, Bolio-Galvis A, Jiménez-Gutiérrez C, Jimenez-Escobar I, López-Velázquez G. Efficacy of lactobacillus reuteri DSM 17938 for infantile colic: systematic review with network meta-analysis. Medicine.2017:96(51).
19. Sung V, D'Amico F, Cabana MD, Chau K, Koren G, Savino F, et al. Lactobacillus reuteri to treat infant colic: a meta-analysis. Pediatrics.2018;141(1):e20171811.
20. Maragkoudaki M, Chouliaras G, Orel R, Horvath A, Szajewska H, Papadopoulou A. Lactobacillus reuteri DSM 17938 and a placebo both significantly reduced symptoms in children with functional abdominal pain. Acta Paediatrica.2017;106(11):1857-1862.
21. Jadresin O, Hojsak I, Misak Z, Kekez AJ, Trbojevic T, Ivkovic L. Lactobacillus reuteri dsm 17938 in the treatment of functional abdominal pain in children: Rct study. Journal of pediatric gastroenterology and nutrition.2017;64(6):925-929.
22. Weizman Z, Abu-Abed J, Binsztok M. Lactobacillus reuteri DSM 17938 for the management of functional abdominal pain in childhood: a randomized, double-blind, placebo- controlled trial. The Journal of pediatrics.2016;17:160-164.
23. Dinleyici EC, Dalgic N, Guven S, Metin O, Yasa O, Kurugol Z Lactobacillus reuteri DSM 17938 shortens acute infectious diarrhea in a pediatric outpatient setting. Jornal de Pediatria (Versão em Português).2015;91(4):392-396.
24. Guarino A, Ashkenazi S, Gendrel D, Vecchio AL, Shamir R, Szajewska H. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition/European Society for Pediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe: update 201. Journal of pediatric gastroenterology and nutrition.2014;59(1):132-152.
25. Urbańska M, Gieruszczak‐Białek D, Szajewska . Systematic review with meta‐analysis: Lactobacillus reuteri DSM 17938 for diarrhoeal diseases in children. Alimentary pharmacology & therapeutics.2016;43(10):1025-1034.
26. Urbańska M, Gieruszczak-Białek D, Szymański H, Szajewska H. Effectiveness of Lactobacillus reuteri DSM 17938 for the Prevention of Nosocomial Diarrhea in Children. The Pediatric infectious disease journal.2016;35(2):142-145.
27. Guarino A, Albano F, Ashkenazi S, Gendrel D, Hoekstra JH, Shamir R, et al. European Society for Paediatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe: executive summary. Journal of pediatric gastroenterology and nutrition.2008;46(5):619-621.
28. Indrio F, Riezzo G, Tafuri S, Ficarella M, Carlucci B, Bisceglia M, et al. Probiotic supplementation in preterm: Feeding intolerance and hospital cost. Nutrients2017;9(9): 965.
29. Belei O, Olariu L, Dobrescu A, Marcovici T, Marginean O. Is It Useful to Administer Probiotics Together With Proton Pump Inhibitors in Children With Gastroesophageal Reflux?. Journal of neurogastroenterology and motility.2018;24(1):51.
30. Rodenas CLG, Lepage M, Ngom-Bru C, Fotiou A, Papagaroufalis K, Berger B. Effect of formula containing Lactobacillus reuteri DSM 17938 on fecal microbiota of infants born by cesarean-section. Journal of pediatric gastroenterology and nutrition.2016;63(6):681-687.
31. Patro-Gołąb B, Szajewska H. Systematic Review with Meta- Analysis: Lactobacillus reuteri DSM 17938 for Treating Acute Gastroenteritis in Children. An Update. Nutrients.2019;11(11).