Número atual: 23(2) - Junho 2023
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
RedLara Pages
Uso do surfactante na doença da membrana hialina por meio de técnica minimamente invasiva em uma unidade neonatal de Belo Horizonte
The use of surfactant for respiratory distress syndrome by minimally invasive technique in a neonatal unit in Belo Horizonte
Felipe Borges Coutinho1; Síura Aparecida Borges Silva1,2; Rachel Pimentel Romano Silveira1; Bruno Vítor Peixoto Militão1; Luciana De Almeida D'Elboux Grizze2
DOI:10.31365/issn.2595-1769.v23i2p49-55
1. Universidade de Itaúna, Faculdade de Medicina - Itaúna - Minas Gerais - Brasil
2. Maternidade Odete Valadares - FHEMIG, Neonatologia - Belo Horizonte - Minas Gerais - Brasil
Endereço para correspondência:
Recebido em: 28/12/2022
Aprovado em: 17/05/2023
Resumo
INTRODUÇÃO: A doença da membrana hialina (DMH), também conhecida como síndrome do desconforto respiratório (SDR) e, contemporaneamente, referida apenas como deficiência de surfactante, é a causa mais comum de desconforto respiratório em bebês prematuros, correlacionando-se com a imaturidade pulmonar estrutural e funcional.
OBJETIVOS: Descrever a experiência da técnica minimamente invasiva de surfactante (MIST) em recém-nascidos (RN) com doença da membrana hialina e avaliar os resultados do protocolo do serviço, definindo possíveis pontos a serem melhorados.
MÉTODOS: Estudo transversal realizado com dados da unidade entre junho de 2018 e fevereiro de 2020. Foram incluídos os RN submetidos a técnica MIST (Prematuros menores de 32 semanas com SDR: FiO2 > 30% para manter saturação entre 90-95% em CPAP). Foram excluídos RN que evoluíram para óbito e transferências.
RESULTADOS: O surfactante foi administrado em doses de 100 a 200 mg/kg, sendo que 47,4% dos RN receberam dentro das primeiras 6 horas de vida e 11,8% nas primeiras 2 horas. A analgesia utilizada foi a não farmacológica com glicose a 25%. Não foram observados efeitos adversos significativos, sendo o refluxo de surfactante o principal deles. Todos os RN submetidos à MIST com menos de 28 semanas evoluíram com displasia broncopulmonar (DBP), sendo 54,5% leve e 45,5% moderada a grave. Nos RN > 28 semanas, 53,5% evoluíram DBP, no entanto, 84,6% de forma leve e apenas 15,4% de forma moderada a grave.
CONCLUSÃO: A MIST foi considerada uma prática segura na assistência de RN prematuros, havendo indicadores do sucesso do protocolo implantado.
Palavras-chave: Doença da Membrana Hialina. Proteína A Associada a Surfactante Pulmonar. Doenças do Prematuro.
Abstract
INTRODUCTION: Hyaline membrane disease (HDM), also known as respiratory distress syndrome (RDS) and, nowadays, just referred to as surfactant deficiency, is the most common cause of respiratory distress in preterm infants, correlating with structural lung immaturity and function.
OBJECTIVES: Describe the experience of the minimally invasive surfactant technique (MIST) in newborns (NB) with respiratory distress syndrome (RDS) and to evaluate the results of the services protocol, defining possible points for improvement.
METHODS: A cross-sectional study carried out with data from the unit between June 2018 and February 2020. Newborns submitted to the MIST technique were included (Premature infants younger than 32 weeks with SDR: FiO2 > 30% to maintain saturation between 90-95% on CPAP). NBs who progressed to death and transfers were excluded.
RESULTS: Surfactant was administered in doses of 100 to 200 mg/kg, and 47.4% of newborns received it within the first 6 hours of life and 11.8% within the first 2 hours. The analgesia used was non-pharmacological with 25% glucose. No significant adverse effects were observed, with surfactant reflux being the main one. All newborns submitted to MIST at less than 28 weeks developed bronchopulmonary dysplasia (BPD), 54.5% of which were mild and 45.5% were moderate to severe. In the NB > 28 weeks, 53.5% developed BPD, however, 84.6% had a mild form and only 15.4% had a moderate to severe form.
CONCLUSION: MIST was considered a safe practice in the care of premature newborns, with indicators of the success of the protocol implemented.
Keywords: Pulmonary Surfactants. Respiratory Distress Syndrome. Newborn. Infant, Newborn. Diseases.
Introdução
A doença da membrana hialina (DMH), também conhecida como síndrome do desconforto respiratório (SDR), é a causa mais comum de desconforto respiratório em bebês prematuros.1,2 Ocorre em 40 mil recém-nascidos (RN) nos Estados Unidos anualmente, sendo mais comum abaixo de 28 semanas de gestação.1,3 A condição é mais prevalente em meninos, e a incidência é aproximadamente seis vezes maior em RN com mães diabéticas, devido ao atraso da maturidade pulmonar.1
A fisiopatologia envolve a maturação incompleta dos pneumócitos tipo II, que são responsáveis por produzir e armazenar surfactante por volta da 22ª semana de gestação.1,3-5 A deficiência de surfactante aumenta a tensão superficial e diminui as trocas gasosas, levando a redução da complacência pulmonar e aumento da incidência de atelectasia alveolar.1,3,4
Clinicamente, caracteriza-se por achados típicos de radiografia de tórax e dependência crônica de oxigênio no RN prematuro.1,6 Está associada a hospitalizações frequentes e prolongadas, especialmente por pneumopatias, altos índices de mortalidade e alterações no desenvolvimento neuropsicomotor e no crescimento pôndero-estatural.7
A reposição de surfactante via tubo endotraqueal é estratégia eficaz na abordagem da SDR, que leva à rápida melhora das trocas gasosas pulmonares, redução do trabalho respiratório, diminuição do risco de edema pulmonar intersticial, pneumotórax e mortalidade.8 Porém, tanto intubação quanto a ventilação mecânica invasiva (VMI), usadas na abordagem convencional, podem gerar lesões em vias respiratórias, aumentando a morbimortalidade em neonatos.9,10 Por essa razão, técnicas menos invasivas têm sido desenvolvidas.
A estratégia INSURE (INtubate, SURfactant, Extubate) foi proposta em países escandinavos e minimizou a duração da ventilação pós-intubação.4,5,11,12 Consiste na intubação, administração de surfactante, rápida extubação e continuação do suporte não invasivo no RN.4,5 Mesmo assim, a intubação implica possível dano à mucosa do epitélio endotraqueal de vias aéreas, bem como o desenvolvimento da DBP.5
Procedimentos menos invasivos foram propostos, como a MIST (Minimally Invasive Surfactant - terapia com surfactante minimamente invasiva) ou LISA (Less Invasive Surfactant Administration). A terapia MIST possui quatro técnicas descritas: instilação de surfactante intrafaríngeo, nebulização de surfactante, instilação por meio de máscara laríngea e instilação por meio de um cateter endotraqueal fino, sendo o último o mais comum.13
Neste estudo, discorre-se sobre a aplicação da técnica MIST por instilação em cateter fino, consistindo na utilização de um laringoscópio e, opcionalmente, de uma pinça Magill para colocação do cateter inserido por via oral ou nasal além das cordas vocais.13,14 O surfactante é administrado lentamente na traqueia enquanto a criança está respirando espontaneamente com suporte respiratório não invasivo.14 À luz de crescentes evidências sobre a superioridade da técnica, diretrizes mundiais recomendaram o MIST como uma alternativa ao INSURE.12 No entanto, há uma escassez de dados sobre a viabilidade do MIST nos países em desenvolvimento,4 como é o caso do Brasil.
Nosso objetivo é descrever a experiência do uso do surfactante em RN com SDR, por meio da técnica MIST, numa unidade de cuidados intensivos neonatais (UTIN) de Belo Horizonte, Minas Gerais.
Metodologia
Trata-se de estudo descritivo do tipo transversal, cujos dados foram obtidos do banco de dados da UTIN da Maternidade Odete Valadares, em Minas Gerais, e de prontuários de RN que receberam surfactante pela técnica MIST, entre os meses de junho de 2018 a fevereiro de 2020. Conforme protocolo interno, foram incluídos no estudo RN prematuros que não apresentaram necessidade de se manterem intubados após reanimação em sala de parto e com SDR caracterizada por sinais radiológicos compatíveis e necessidade de fração inspirada de oxigênio (FiO2) > 30% para manter saturação entre 90-95% em pressão positiva contínua nas vias aéreas (CPAP). Foram excluídos da amostra RN que evoluíram para óbito e os que foram transferidos para outra unidade hospitalar.
A administração do surfactante porcino, padronizado no serviço (Curosurf® 240mg/3ml), é feita na dose de 100 a 200 mg/kg, via TOT nº 2, sonda uretral nº 6 ou 8 (conforme habilidade do neonatologista de plantão), em alíquota única, vagarosamente, com o RN em CPAP nasal. Após a administração, o RN é mantido em CPAP com pressão positiva expiratória final (PEEP) de 6-7 mmHg e FiO2 suficiente para manter saturação entre 90 e 95%.
Analgesia com glicose a 25% foi realizada, e a cafeína foi iniciada tão logo que possível na dose de ataque de 20 mg/kg, seguida de 5 mg/kg de manutenção a cada 24 horas. Considera-se como falha da MIST a necessidade de intubação do RN por apresentar piora do esforço respiratório avaliado pelo Boletim de Silverman Andersen (BSA ≥ 6) e/ou necessidade de FiO2 > 60%, a qualquer momento.
Para caracterização da amostra, foram analisados: peso de nascimento, idade gestacional, sexo, uso de corticoide antenatal, tipo de parto, Apgar de 1º e 5º minutos, reanimação em sala de parto. Para análise da técnica MIST: tempo de administração do surfactante, uso de sonda ou tubo orotraqueal para administração, intercorrências clínicas durante a administração, uso de medidas sedo-analgésicas, dose do surfactante, necessidade de doses adicionais de surfactante, necessidade de intubação posterior ao procedimento, tempo de ventilação mecânica na intubação, tempo de uso de CPAP (idade cronológica e pós-natal de suspensão), suporte ventilatório no 28º dia de vida e na 36º semana gestacional corrigida dos RN, para diagnóstico da DBP e de sua gravidade, respectivamente.
Considerou-se como diagnóstico de DBP a necessidade de oxigenioterapia aos 28 dias de vida. A gravidade da DBP foi avaliada com 36 semanas de idade gestacional corrigida (IGCo). Foi classificada como leve se, com essa IGCo, o RN estava em ar ambiente; moderada, se necessitava de FiO2 menor que 30% em cateter nasal, CPAP ou VNI; e grave, se o RN se encontrava em VMI ou com FiO2 maior que 30% em CPAP ou VNI.
Para avaliação das informações, foram realizados análise da frequência e cálculo da média dos dados quando pertinentes.
A assinatura do Termo de Consentimento Livre e Esclarecido não foi solicitada, pois o estudo utilizou exclusivamente dados de prontuário. A presente pesquisa foi aprovada pelo Comitê de Ética da Fundação Hospitalar de Minas Gerais.
Resultados
As características perinatais da amostra dos RN analisados estão expostas na Tabela 1. Um total de 65 RN foi submetido a técnica do MIST entre julho de 2018 e janeiro de 2020. No entanto, 5 RN foram excluídos, 2 por óbito devido a sepse tardia e 4 por terem sido transferidos de hospital.
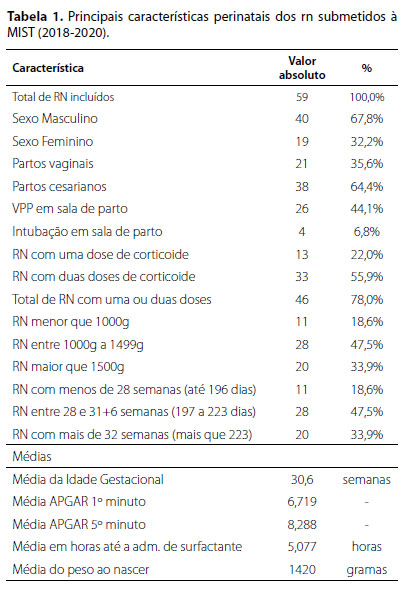
A via de parto predominante foi a cesárea (64,4%) e as principais indicações foram a hipertensão materna e sofrimento fetal agudo ou crônico, incluindo retardo de crescimento intraútero.
O surfactante foi administrado por meio de sonda uretral 06, 08 e tubo orotraqueal nº 2 em doses que variaram de 100 a 200 mg/kg. Analgesia não farmacológica com glicose a 25% foi utilizada em alguns RN, a critério do plantonista. O único efeito adverso observado foi o refluxo do surfactante.
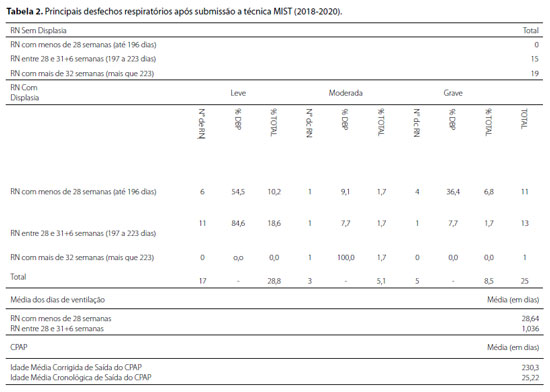
Em relação aos desfechos respiratórios analisados (Tabela 2), 34 RN (57,6%) não apresentaram displasia, todos acima de 28 semanas, enquanto 100% de RN menores de 28 semanas evoluíram com a doença. Apenas um RN maior que 32 semanas evoluiu com DBP. A gravidade da displasia variou entre os grupos, sendo que os casos graves predominaram na faixa de menor idade gestacional.
Houve falha da MIST em 16 RN (27,1%), com necessidade de intubação e VM. O tempo de VM foi de até 3 dias em 10,1%; de 8 a 21 dias em 10,1%; e maior que 21 dias em 4 RN. Entre os 16 RN com falha da MIST, 50% tinham menos de 28 semanas e 43,7% tinham menos de 1.000g; a intersecção entre os dois fatores corresponde a 37,5%; e os tempos mais longos de VM foram observados neste grupo (média 28,6 dias para os < 28 semanas e 1,0 dia para os de 28 a 31+6 semanas).
A idade gestacional média de suspensão do CPAP em RN que tiveram boa evolução após a MIST foi de 32 a 33 semanas, e a cronológica, de 25, 2 dias entre todos os RN, sendo que a maioria desses RN permaneceu em ar ambiente.
Discussão
O objetivo deste estudo foi descrever a experiência de administração do surfactante pela MIST e avaliar o protocolo proposto em nossa UTIN, definindo possíveis pontos a serem melhorados. Além disso, espera-se contribuir com outros serviços que desejem implantar essa estratégia de tratamento para SDR.
A amostra observada consta de 59 RN, sendo 40 do sexo masculino (67,8%) e 19 do feminino (32,2%). A prevalência do sexo masculino coincide também com os dados epidemiológicos da DBP.1 Entretanto, estudos semelhantes ao nosso mostraram proporções iguais em suas amostras.17-19
A administração da MIST em RN de IG entre 28 e 31+6 semanas foi a mais encontrada em várias referências analisadas.4,15,17,18,20 Em nossos RN, a IG média foi de 30 semanas e 4 dias. Na amostra, 18,6% tinham menos de 28 semanas, 62,7% entre 28 e 31+6 e 18,6% 32 ou mais semanas de IG.
A idade gestacional é o fator de risco mais importante para SDR, e a maioria dos casos tende a ocorrer em IG mais baixas.16 Embora nosso protocolo preveja a realização da MIST em RN abaixo de 28 semanas, observamos menor número de administrações nesses RN prematuros. Há estudos descrevendo a aplicação da MIST, inclusive em RN bem imaturos (<25 semanas), ou até protocolos específicos profiláticos da MIST já aos 20 minutos de vida nesse grupo.21,22
Assim, considerando a sobrevida cada vez maior desses prematuros extremos, o uso da MIST, juntamente com o clampeamento tardio do cordão e uso do CPAP precoce, está entre boas medidas de suporte menos invasivo.19,22,23
Alguns autores não indicam a MIST para RN maiores de 32 semanas, pelo risco de DBP ser baixo e, de nessa faixa de IG, haver maior necessidade de sedação/analgesia para execução da técnica, o que poderia comprometer os resultados.22,24,25 O peso de nascimento médio no nosso estudo foi de 1.420 gramas, sendo que 18,6% tinham menos de 1.000g e 47,5% entre 1.000 e 1.499g. Médias de pesos inferiores foram observados em outros estudos em que se utilizou a MIST.17,18
Ao avaliarmos os dados relacionados à gestação, 78% das mães desses RN receberam pelo menos uma dose de corticoide antes do parto, sendo que 55,9% receberam esquema completo de 2 doses pré-natal. A maturação pulmonar pré-natal com corticosteroides é importante para a respiração espontânea logo após o nascimento, fator importante que pode garantir o sucesso da técnica e diminuir a incidência e a gravidade da SDR.16,22
A maior prevalência da cesariana em nossa amostra pode ser explicada pelas principais causas de prematuridade levantadas. Padrão semelhante é encontrado na literatura.17,18
No presente estudo, a nota média de Apgar de 1º minuto foi 6,7 e de quinto minuto, de 8,2. Cerca de metade dos RN apresentou Apgar menor que 7 no primeiro minuto e 98% Apgar maior que 7 no quinto minuto, demonstrando boa resposta às medidas de reanimação. Esse parâmetro é definitivo para a realização da técnica em nossa UTIN, pois apenas os RN que não permanecem intubados após a reanimação em sala de parto são candidatos à MIST. Além disso, pode estar correlacionado à melhor resposta à técnica. A melhora na resposta do Apgar do 1º ao 5º minuto também é observada em outras UTIN.17,18,20 Apenas em 4 pacientes (6,8%) a intubação endotraqueal para reanimação foi necessária, já a VPP foi utilizada em 25 RN (42,4%).
A dose de surfactante utilizada variou de 100 a 200 mg/kg. Os dados coincidem com a maioria dos estudos acerca da MIST, nos quais a dose máxima de surfactante bovino ou suíno observada não ultrapassou 200mg/kg.4,11,15,17,18,20,22,23 Estima-se que uma dose maior resulte em menor necessidade de retratamento, que pode ocorrer em até 20 a 30% dos RN submetidos à técnica.22
Em nossa experiência, 47,4% receberam surfactante pelo MIST entre 4 e 6 horas de vida, e destes, 11,8% com até 2 horas de vida. A literatura aponta que a administração precoce, nas primeiras 2 horas de vida, tende a ser melhor do que a administração tardia de surfactante, levando a um menor risco de DBP ou extravasamento de ar pulmonar.16,26
Acreditamos que a necessidade de estabilização do RN e medidas iniciais, como instituição de acesso venoso e realização de radiografia de tórax, sejam os principais fatores de atraso na realização da técnica e devem ser agilizados, para que se atinja o tempo ideal de administração para a maioria dos prematuros. Nesse sentido, a existência de protocolos de admissão e de indicações precisas para a técnica pode contribuir para o alcance desse objetivo.
Em nosso protocolo, não foi utilizada analgesia medicamentosa. A glicose a 25% e a contenção do RN foram usadas em nossos RN como analgesia não farmacológica, de forma similar ao uso das soluções de sacarose na maioria dos centros.15 Isso porque, embora o uso de analgésicos e sedativos convencionais, principalmente o fentanil, cetamina e o propofol, ajude a reduzir os escores de dor, ele também pode interferir na respiração espontânea.15,20
O uso da cafeína é realizado para estimulação da respiração já na sala de parto, embora não haja ensaios clínicos randomizados que apoiem essa abordagem.22 Em nossa instituição, todos os RN submetidos à MIST usaram cafeína após a sua realização, conforme protocolos similares de outras UTIN.
O refluxo do surfactante, intercorrência observada também em nossa experiência, é comum pelo fato de o cateter não preencher totalmente a laringe e refluir para a cavidade oral.17 Complicações nas técnicas MIST têm-se mostrado menos frequentes, o que encoraja cada vez mais sua implementação.18 Entre os efeitos adversos, a literatura cita risco de perfuração intestinal, engasgos, bradicardia, apneia, dessaturações e diminuição da oxigenação cerebral. Tais efeitos estão mais associados à laringoscopia para administração do surfactante.19,23,27,28
Em relação à evolução dos RN, observou-se que a maioria deles, após a técnica MIST, permaneceu em CPAP ou ventilação não invasiva (VNI), com FiO2 inferior a 30%, configurando sucesso da técnica. Apenas 8,4% necessitaram de uma segunda dose de surfactante e estabilizaram o quadro após as mesmas. Houve falha da MIST em 27,1% dos RN, que foram intubados e permaneceram em ventilação mecânica por um período que variou de 1 a 106 dias, sendo necessária nova administração de surfactante. A necessidade de segunda dose é possível entre RN que apresentam melhora respiratória temporária após a primeira dose e evidência radiológica de síndrome do desconforto respiratório em curso.18,23
Observamos diferença no tempo de VM dos RN submetidos à MIST e em que houve falha da técnica com necessidade de intubação, quando comparados com RN submetidos à administração convencional de surfactante em nosso próprio serviço. O tempo médio de VM foi semelhante entre os dois grupos de RN menores de 28 semanas, porém foi menor com a técnica MIST em RN com IG entre 28 e 32 semanas. Nessa faixa de IG, o tempo médio de VM diminuiu de 4 dias no método convencional para um dia nos RN submetidos à MIST, demonstrando um efeito positivo entre esses RN. Em um outro estudo, com 47 lactentes de 28 a 31+6 semanas submetidos à MIST, a média de dias de VM foi superior à observada no nosso estudo, de 6,8 dias.18
Há controvérsias na literatura sobre a IG ideal para suspensão do CPAP. Os estudos mais tradicionais no uso de CPAP de bolha consideram que é raro o desmame antes de 32 semanas de IG e que, em média, é continuado até 34,5 semanas.29
Na nossa pesquisa, a IG de suspensão do CPAP após a MIST foi de 32 a 33 semanas, sendo que a maioria permaneceu em ar ambiente, sem dependência de oxigênio por cateter nasal, o que consideramos resultado favorável. Utilizamos como critério de suspensão do CPAP uma IG mínima de 32 semanas; PEEP de 5 cmH2O; FiO2 de 21% e ausência de episódios significativos de apneia e de esforço respiratório nas últimas 24 horas. Esses critérios coincidem com os de outras publicações.20.
A relação da técnica MIST e DBP tem sido relatada em vários estudos.5,11-15,17,22-24 Em nossa observação, todos os RN submetidos à MIST com menos de 28 semanas evoluíram com DBP, sendo que 54,5% foram classificados como leve; e 45,5%, moderada a grave. Em resultados anteriores do nosso serviço, na técnica convencional, os menores de 28 semanas cursaram com DBP moderada a grave em uma prevalência consideravelmente maior (71,4%).
Entre os RN de 28 a 31+6, na experiência atual, DBP ocorreu em 53,5% dos casos. Destes, 84,6% foram de intensidade leve; e 15,4%, de intensidade moderada a grave. Na observação anterior, em nossa UTIN, 23,4% dos RN receberam a técnica convencional e evoluíram com DBP moderada a grave. Tais resultados demonstram menor prevalência de casos graves em RN submetidos à MIST.
No maior ensaio clínico realizado até o momento, com 485 lactentes entre 25 e 28 semanas, a técnica MIST pareceu não implicar alterações nos desfechos primários analisados (displasia broncopulmonar e morte).24 No entanto, evidenciou de maneira robusta a redução de desfechos secundários, principalmente no que se refere à redução de tempo de tratamento e aos próprios efeitos adversos da técnica convencional.24 No que tange à gravidade da DBP, os estudos ainda parecem obscuros e, por essa razão, torna-se interessante a experiência aqui relatada.
Metanálises apontam que o MIST é superior ao CPAP sozinho ou à técnica INSURE, tanto em termos de prevenção de DBP quanto de hemorragia intracraniana.23 No entanto, a qualidade de alguns dos estudos incluídos nessas metanálises ainda é questionável, de modo que ainda são necessários mais estudos randomizados controlados confirmativos.22 Pesquisas em animais e ensaios clínicos piloto têm observado vantagens teóricas das técnicas minimamente invasivas.23
Conclusões
Consideramos que a implantação da MIST demonstrou ser uma prática segura e eficiente na assistência de RN prematuros e pode abranger também prematuros extremos. A revisão periódica de eventos adversos durante a administração do surfactante, bem como o tempo de administração do surfactante, as falhas da estratégia, a prevalência e a gravidade da displasia broncopulmonar podem ser bons indicadores do sucesso do protocolo implantado.
Agradecimentos
Agradecemos à Maternidade Odete Valadares, por fornecer e permitir o uso dos dados na pesquisa, e à equipe multiprofissional da Unidade de Terapia Intensiva Neonatal que, de alguma forma, contribuiu e incentivou a realização desta pesquisa.
Referências
1. Hermansen CL, Lorah KN. Respiratory Distress in the Newborn Table 1. Differential Diagnosis of Respiratory Distress in the Newborn. Vol. 76. 2007.
2. Malloy MH, McGovern JP. Hyaline membrane disease (HMD): an historical and Oslerian perspective. J Perinatol. 2018;38:1602-6.
3. Rubarth LB, Quinn J. Respiratory Development and Respiratory Distress Syndrome. Neonatal Netw. 2015;34:231-8.
4. Gupta BK, Saha AK, Mukherjee S, Saha B. Minimally invasive surfactant therapy versus InSurE in preterm neonates of 28 to 34 weeks with respiratory distress syndrome on non-invasive positive pressure ventilation-a randomized controlled trial. Eur J Pediatr. 2020;179:1287-93.
5. Han T, Liu H, Zhang H, Guo M, Zhang X, Duan Y, et al. Minimally Invasive Surfactant Administration for the Treatment of Neonatal Respiratory Distress Syndrome: A Multicenter Randomized Study in China. Front Pediatr. 2020;8:182.
6. Fischer HS, Bührer C. Avoiding endotracheal ventilation to prevent bronchopulmonary dysplasia: A meta-analysis. Pediatrics. 2013;132:e1351-60.
7. Góngora JJG. Displasia broncopulmonar. Rev Mex Pediatr. 2010;77:27-37.
8. Rojas-Reyes MX, Morley CJ, Soll R. Prophylactic versus selective use of surfactant in preventing morbidity and mortality in preterm infants. Cochrane Database Syst Rev. 2012;2012.
9. NN F, WA C, MC W, W R, MG G, AR L, et al. Early CPAP versus surfactant in extremely preterm infants. N Engl J Med. 2010;362:1970-9.
10. Dunn MS, Kaempf J, De Klerk A, De Klerk R, Reilly M, Howard D, et al. Randomized trial comparing 3 approaches to the initial respiratory management of preterm neonates. Pediatrics. 2011;128.
11. Gengaimuthu K. Minimally Invasive Surfactant Therapy: An Analytical Report of Our Prospective Dubai Cohort. Cureus. 2020;12.
12. Wang XA, Chen LJ, Chen SM, Su PH, Chen JY. Minimally invasive surfactant therapy versus intubation for surfactant administration in very low birth weight infants with respiratory distress syndrome. Pediatr Neonatol. 2020;61:210-5.
13. Shim GH. Update of minimally invasive surfactant therapy. Korean J Pediatr. 2017;60:273-81.
14. Klotz D, Porcaro U, Fleck T, Fuchs H. European perspective on less invasive surfactant administration-a survey. Eur J Pediatr. 2017;176:147-54.
15. Herting E, Härtel C, Göpel W. Less invasive surfactant administration (LISA): chances and limitations. Arch Dis Child Fetal Neonatal Ed. 2019;104:F655.
16. Eichenwald EC, Stark AR. Bronchopulmonary dysplasia: Definition, pathogenesis, and clinical features - UpToDate. UpToDate. 2022.
17. Kaniewska U, Gulczyńska E. The influence of the technique of surfactant administration (LISA vs INSURE) on the outcomes of respiratory distress syndrome treatment in preterm infants. Dev Period Med. 2019;23:163-71.
18. Bao Y, Zhang G, Wu M, Ma L, Zhu J. A pilot study of less invasive surfactant administration in very preterm infants in a Chinese tertiary center. BMC Pediatr. 2015;15.
19. Härtel C, Paul P, Hanke K, Humberg A, Kribs A, Mehler K, et al. Less invasive surfactant administration and complications of preterm birth. Sci Rep. 2018;8.
20. Zhu J, Bao Y, Du L, Huang H, Lv Q, Jiang Y, et al. Less invasive surfactant administration versus endotracheal surfactant instillation followed by limited peak pressure ventilation in preterm infants with respiratory distress syndrome in China: study protocol for a randomized controlled trial. Trials. 2020;21.
21. Mehler K, Oberthuer A, Keller T, Becker I, Valter M, Roth B, et al. Survival Among Infants Born at 22 or 23 Weeks' Gestation Following Active Prenatal and Postnatal Care. JAMA Pediatr. 2016;170:671-7.
22. Herting E, Härtel C, Göpel W. Less invasive surfactant administration: best practices and unanswered questions. Curr Opin Pediatr. 2020;32:228-34.
23. Härtel C, Glaser K, Speer CP. The Miracles of Surfactant: Less Invasive Surfactant Administration, Nebulization, and Carrier of Topical Drugs. Neonatology. 2021;118:225-34.
24. Dargaville PA, Kamlin COF, Orsini F, Wang X, Paoli AG De, Kutman HGK, et al. Effect of Minimally Invasive Surfactant Therapy vs Sham Treatment on Death or Bronchopulmonary Dysplasia in Preterm Infants With Respiratory Distress Syndrome: The OPTIMIST-A Randomized Clinical Trial. JAMA. 2021;326:2478-87.
25. Dargaville PA, Ali SKM, Jackson HD, Williams C, De Paoli AG. Impact of Minimally Invasive Surfactant Therapy in Preterm Infants at 29-32 Weeks Gestation. Neonatology. 2018;113:7-14.
26. Laughon MM, Langer JC, Bose CL, Smith PB, Ambalavanan N, Kennedy KA, et al. Prediction of Bronchopulmonary Dysplasia by Postnatal Age in Extremely Premature Infants. Am J Respir Crit Care Med. 2011;183:1715.
27. Ambulkar H, Williams EE, Hickey A, Bhat R, Dassios T, Greenough A. Respiratory monitoring during less invasive surfactant administration in the delivery suite. Early Hum Dev. 2021;154:105311.
28. Hanke K, Rausch TK, Paul P, Hellwig I, Krämer C, Stichtenoth G, et al. The effect of less invasive surfactant administration on cerebral oxygenation in preterm infants. Acta Paediatr. 2020;109:291-9.
29. Bamat N, Jensen EA, Kirpalani H. Duration of continuous positive airway pressure in premature infants. Semin Fetal Neonatal Med. 2016;21:189-95.