Número atual: 13(2) - Dezembro 2012
Sem Seçao
Asma aguda na infância
Terezinha Miceli Martire
Professora associada do Setor de Pneumologia Pediátrica do Serviço de Pediatria da Universidade Federal do Estado do Rio de Janeiro - UNIRIO. Presidente do Comitê de Doenças do Aparelho Respiratório da Sociedade de Pediatria do Estado do Rio de Janeiro - SOPERJ 2010-2012. Presidente do Departamento de Pneumologia Pediátrica da ALAT 2012-2014
DEFINIÇÃO E ASPECTOS EPIDEMIOLÓGICOS
A asma é uma doença inflamatória crônica, predominantemente eosinofílica, caracterizada por distúrbio ventilatório obstrutivo de graus variados, sendo uma das principais causas de visita às salas de emergência pediátrica nas unidades hospitalares. Manifesta-se clinicamente por episódios recorrentes de sibilância, dispnéia, sensação de aperto no peito e tosse, particularmente à noite e ao despertar. Hoje, sabe-se que existem diversas apresentações clínicas, que se diferem de acordo com o fenótipo do paciente. É um resultado da interação entre genética, exposição ambiental precoce à aeroalérgenos e outros fatores que causam o desenvolvimento e a manutenção dos sintomas.
É a doença crônica mais prevalente na infância, acometendo, só nos Estados Unidos, 7 milhões de crianças. Nos últimos 25 anos, a taxa de prevalência dobrou em todo o mundo. No Brasil, ocorrem cerca de 300 mil internações/ano, incluindo adultos e crianças, constituindo-se na 3ª causa de hospitalização, segundo dados do DATASUS (2008). Estudo multicêntrico (International study for asthma and allergies in childhood - ISAAC) apontou ser a prevalência média mundial de asma 11,6% entre escolares (6 e 7 anos), oscilando entre 2,4 e 37,6%. Entre os adolescentes (13 e 14 anos), a prevalência mundial média foi de 13,7% e oscilou entre 1,5 e 32,6%. No Brasil, em algumas cidades, os índices ainda permanecem elevados ao redor de 20%, para as duas faixas etárias.
A mortalidade por asma ainda é baixa, mas apresenta magnitude crescente em diversos países. Nos países em desenvolvimento, a mortalidade vem aumentando nos últimos 10 anos, correspondendo a 5 a 10% das mortes por causa respiratória, com elevada proporção de óbitos domiciliares.
Apesar dos casos de asma grave serem apenas 5 a 10% do total de pacientes com asma, apresentam maior morbimortalidade relativa e são responsáveis por um consumo desproporcionalmente alto dos recursos de saúde em relação aos grupos de menor gravidade. Pacientes com asma grave não controlada procuram 15 vezes mais as unidades de emergência médica e são hospitalizados 20 vezes mais do que asmáticos moderados.
Reconhece-se, portanto, a importância de se fazer o diagnóstico precoce, classificar o paciente de acordo com a gravidade e evitar as exacerbações na faixa etária pediátrica e de adolescente. Tais medidas permitirão mudar o retrato das emergências no Brasil, visando à diminuição da morbimortalidade dessa doença crônica, permitindo seu controle e, quando possível, impedindo sua evolução para distúrbios ventilatórios obstrutivos de diferentes níveis de gravidade.
EXACERBAÇÃO AGUDA DA ASMA NA CRIANÇA
Conceito
A exacerbação é um episódio agudo ou subagudo de progressiva dificuldade respiratória com tosse, sibilância e dor ou desconforto torácico ou combinação de todos esses sintomas, acompanhada por diminuição ao fluxo expiratório, que pode ser quantificado por medidas de função pulmonar e ou de O2.
A crise aguda de asma ou exacerbação aguda da asma é um evento que requer imediata ação tanto por parte do paciente (ou responsável) quanto por parte do médico, de modo a evitar desfechos como hospitalização, internação em UTI e até óbito. A ocorrência da crise aguda é um marcador de inadequado controle da doença. A ATS/ERS (American Thoracic Society/ European Respiratory Society) define exacerbação como mudança do quadro respiratório prévio em que o paciente se encontrava.
Gravidade
A gravidade, por sua vez, pode ser estratificada de acordo com a idade da criança:
Crianças de 0 a 4 anos
Identifica-se a gravidade por sinais e sintomas (uso de musculatura acessória, sibilos inspiratórios e expiratórios, respiração paradoxal, cianose, taquidispneia, tosse, letargia ou agitação psicomotora, pouca tolerância ao exercício, atividades diárias prejudicadas) e pelo escore pediátrico de gravidade da asma, além da necessidade do uso de β2 agonista, de corticoide sistêmico ou aumento do esteroide inalatório. Entre as medidas objetivas, a de maior relevância é a saturação do O2: que se for < 91% significa dificuldade respiratória grave.
Crianças entre 5 a 11 anos
Todos os sinais e sintomas da criança de 0 a 4 anos, incluindo uma mensuração da função pulmonar - seja por meio do VEF1 (volume expiratório forçado no 1º segundo) ou do PFE (pico de fluxo expiratório).
Por outro lado, o National Institute of Health (NIH) define a exacerbação ou crise aguda de asma de acordo com 3 componentes, todos relacionados a tratamento: (i) uso de esteroide sistêmico, (ii) ida à emergência ou hospitalização e (iii) uso frequente de β2 de curta duração.
Qualquer que seja a definição, a gravidade inicial na apresentação clínica ou laboratorial e a resposta ao tratamento definirá qual a melhor abordagem para o manejo do paciente pediátrico ou do adolescente com crise aguda de asma.
O manejo rápido e eficiente da crise pode alterar favoravelmente o desfecho clínico do paciente, por meio da abordagem sistematizada e diferenciada nos serviços de emergência.
A morbimortalidade nas UTIs se deve a anoxia na maioria das vezes. A intervenção de forma apropriada, com terapia farmacológica agressiva e ventilação mecânica, resulta em um desfecho favorável em alguns casos de exacerbação aguda de asma grave.
FISIOPATOLOGIA
Os processos fisiopatológicos que alteram a função pulmonar na asma grave com risco de vida são: contração da musculatura lisa brônquica, edema, inflamação da mucosa brônquica e obstrução de vias respiratórias. A obstrução do fluxo de ar causa alteração da ventilação/ perfusão e hipoxemia. A obstrução expiratória diminui o VEF1. A principal característica da asma é a diminuição da relação volume expiratório forçado/capacidade vital forçada (VEF1/CVF). Na crise aguda de asma, o paciente é incapaz de completar a expiração devido à resistência expiratória. A taquipneia induzida por limitado tempo expiratório, ocasiona aprisionamento de ar, aumento da capacidade residual funcional e diminuição da CVF.
A hiperinsuflação aumenta o trabalho respiratório. Edema e secreções das vias respiratórias também aumentam e comprometem o fluxo inspiratório, quando combinados com a hiperinsuflação pulmonar.
As causas da parada cardiorrespiratória em pacientes asmáticos geralmente são falha dos músculos inspiratórios, fadiga, hipoxia e, por conseguinte, parada ventilatória. Os achados característicos da asma aguda são vias respiratórias com infiltração de eosinófilos, degranulação de mastócitos, espessamento da membrana basal, perda da integridade das células epiteliais, oclusão da luz brônquica por muco, hiperplasia e hipertrofia da musculatura lisa brônquica e hiperplasia de células caliciformes. Na asma quase fatal ou de difícil controle, o processo inflamatório crônico tem uma maior participação de neutrófilos do que de eosinófilos.
A asma é uma resposta inflamatória evidenciada pela presença de citocinas que medeiam a inflamação. Algumas citocinas iniciam a resposta inflamatória por meio da ativação de fatores de transcrição, que atuam sobre os genes que codificam citocinas inflamatórias, quimiocinas, moléculas de adesão e outras proteínas que induzem e perpetuam a inflamação. A presença de anticorpos IgE em alguns casos está ligada à gravidade da asma. A liberação de citocinas depende da ligação de IgE ao alérgeno. Os anticorpos IgE são sintetizados e liberados pelas células B, que logo circulam no sangue e se ligam a receptores de alta e de baixa afinidade de IgE.
A fase imediata da crise aguda de asma (dentro de 1 hora) caracteriza-se pela inalação do alérgeno, o que causa constrição aguda dos músculos lisos devido à liberação de histaminas e leucotrienos dos mastócitos. A fase prolongada tardia (4 a 6 horas mais tarde) ocorre como um resultado de citocinas e quimiocinas geradas por células inflamatórias residentes (mastócitos, macrófagos, células epiteliais) e células inflamatórias (linfócitos recrutados e eosinófilos), que provocam obstrução adicional ao fluxo respiratório. O interferon-γ encontra-se elevado durante a fase aguda da asma grave, contribuindo para a ativação de eosinófilos e provável aumento da inflamação. Existem dois tipos de células auxiliares de linfócitos CD4 : T Helper de tipo 1 (células TH1), que produzem interleucinas (IL) -2 e interferon-γ, essenciais para os mecanismos de defesa celular. Células auxiliares T de tipo 2 (TH2) produzem as citocinas (IL-4, IL-5, IL-6, IL-9 e IL-13) que medeiam a inflamação. O equilíbrio entre a resposta de citocinas TH1 e TH2 contribui para a causa e evolução das doenças atópicas, incluindo a asma. O sistema imunológico do recém-nascido é predominante de células TH2, e um estímulo oportuno e adequado ambiental é necessário para criar uma resposta imunológica balanceada. A alteração no número de infecções no início da vida, o uso indiscriminado de antibióticos, a adoção do estilo de vida ocidental e a exposição repetida aos alérgenos no lactente podem afetar o equilíbrio entre TH1 e TH2 de citocinas e aumentar a probabilidade de resposta imune de células do tipo TH2 e provocar asma. As evidências mostram a importância dos fatores imunes no desenvolvimento da asma e do resultante processo inflamatório.
Esse processo inflamatório complexo está envolvido tanto nas alterações funcionais, quanto no aparecimento dos sintomas característicos da doença. A broncoconstrição intermitente e reversível é responsável pelas alterações clínicas e está relacionada à contração exagerada do músculo liso brônquico, ao edema da mucosa, às alterações das vias respiratórias decorrentes do remodelamento e à hipersecreção de muco. Acompanham o processo inflamatório alterações estruturais conhecidas como remodelamento das vias respiratórias, presentes desde as fases iniciais da doença e que podem tardiamente contribuir para o estreitamento irreversível das vias respiratórias.
A rede de células dendríticas se abriga entre as células epiteliais das vias respiratórias e lança seus dendritos para a luz brônquica a fim de captar antígenos, processá-los e apresentar peptídeos relevantes para os linfócitos T nos órgãos linfoides periféricos, fazendo a ponte entre a imunidade inata e adaptativa. As células dendríticas cumprem assim um papel central na ativação de linfócitos TH2 e no início da cascata de ativação da inflamação alérgica, presente na maioria dos portadores de asma atópica. Por outro lado, as células dendríticas respiratórias podem induzir a ativação de células T regulatórias (Tregs) e de células TH1, que poderão prevenir o desenvolvimento de reações imunes prejudiciais ao brônquio. Esse conhecimento despontará no futuro delineando importantes alvos terapêuticos para o controle da asma.
FATORES DESENCADEANTES
Os fatores desencadeantes são múltiplos. Em crianças, as infecções virais em menores de 2 anos e os aeroalérgenos nos maiores de 2 anos são os principais estímulos causadores de hiperreatividade brônquica. Entretanto, diversos estímulos são desencadeantes de asma atópica e não atópica:
Alérgenos inalatórios. Infecção viral das vias respiratórias superiores (VRS) ou infecção de vias respiratórias inferiores (VRI) no período de lactância e no pré-escolar. Mudanças climáticas. Exercício físico. Medicamentos. Muito raramente: infecções respiratórias bacterianas, DRGE, alimento, menstruação e gestação.
FATORES DE RISCO PARA GRAVIDADE DA ASMA
A presença de comorbidades deve deixar o pediatra de alerta quanto à gravidade e às complicações decorrentes de uma crise aguda, quando esta ocorre em pacientes portadores de uma ou mais das condições clínicas mencionadas a seguir:
Prematuridade e/ou baixo peso ao nascer. Broncodisplasia pulmonar. Cardiopatia congênita com hiperfluxo pulmonar. Imunodeficiência primária ou secundária. Sexo masculino no pré-púbere e sexo feminino na pós-puberdade. Tabagismo passivo ou ativo.
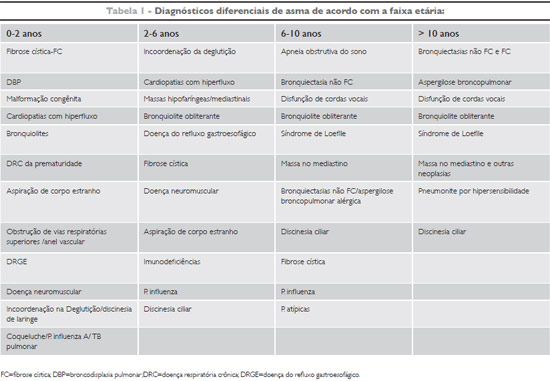
DIAGNÓSTICO DIFERENCIAL
Outros diagnósticos devem ser considerados além de asma e devem ser discutidos se a criança apresentar sibilância recorrente acompanhada de alguns dos sinais clínicos e ou laboratoriais a seguir:
Curva pondero-estatural abaixo do percentil 3. Sopro cardíaco patológico. Baqueteamento digital. Sinais respiratórios unilaterais. Persistência de tosse por mais de 3 semanas. Infecção recorrente de vias aéreas respiratórias superiores e inferiores documentadas por médico.
Nessas circunstâncias, os seguintes diagnósticos devem ser considerados, de acordo a faixa etária.
DIAGNÓSTICO CLÍNICO
O diagnóstico clínico de asma deve ser pensado diante de todos os casos de paciente com queixa de chiado no peito e/ou dor torácica acompanhada de tosse seca assim como 1 ou mais idas às emergências no mês, tosse durante ou imediatamente após exercício físico, sibilância desencadeada por aeroalérgenos, medicamentos e mudanças climáticas, resfriados frequentes acompanhados de chiado e tosse seca persistente. No lactente, consideramos o diagnóstico de asma, diante de mais de 3 episódios de chiado dentro dos primeiros 2 anos de vida e que melhoram com medicação para asma.
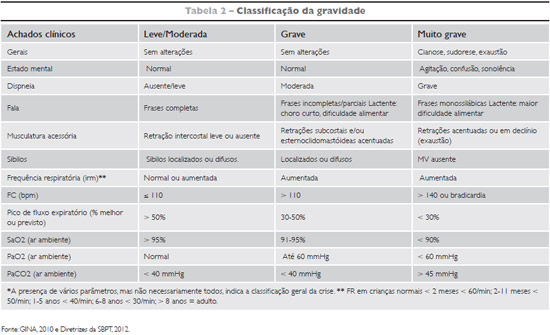
CLASSIFICAÇÃO
A classificação da asma brônquica deve ser baseada nos seguintes fatores: estado mental, taquipneia e/ou dispneia, frequência cardíaca, respiratória, uso de musculatura acessória, saturação de O2 e medida de função pulmonar (na emergência). Classificações com base na gravidade foram concebidas com o objetivo principal de melhorar a abordagem no tratamento. A asma grave pode se tornar um grande problema clínico que exige cuidados especializados e diferentes abordagens no tratamento, desde medicação até ventilação não invasiva (VNI) ou invasiva (VMI).
Os sinais de gravidade baseiam-se na frequência cardíaca e respiratória e no resultado da oximetria. Os sinais clínicos que se seguem devem ser registrados e observados, denotando gravidade: dificuldade de alimentar, taquidispneia, tiragem, uso de musculatura acessória, cianose, palidez, agitação psicomotora e dificuldade na fala. Outros sinais de piora: desidratação, vômito, apneia.
A frequência cardíaca é um fator importante. A taquicardia normalmente evidencia piora do quadro de asma, e a bradicardia mostra deterioração rápida do quadro clínico, tornando necessária a hospitalização. Classificar o paciente de acordo com a gravidade possibilita a definição dos passos iniciais tão logo o paciente chegue à unidade hospitalar, assim como conhecer a medicação que estava sendo utilizada nas 24 horas prévias à internação na emergência.
DIAGNÓSTICO LABORATORIAL
A saturação de oxigênio arterial medida por oximetria de pulso pode ajudar a determinar a gravidade inicial da doença. A medida dos gases arteriais deve ser verificada nos casos em que há sinais de deterioração clínica, fadiga muscular ou risco de falência respiratória iminente, isto é, quando há piora dos sinais de gravidade. O hemograma, por sua vez, só tem indicação quando há suspeita de pneumonia associada.
As radiografias de tórax geralmente não são úteis para o diagnóstico de asma aguda, já que comumente mostram hiperinsuflação pulmonar. Só devem ser feitas para avaliar comorbidades ou complicações. O eletrocardiograma (ECG) deve ser realizado em pacientes com suspeita de distúrbio de ritmo cardíaco.
TRATAMENTO
Pediatras devem educar os pais no reconhecimento precoce e no tratamento das exacerbações das crises agudas de asma, o qual deve ser iniciado em casa e imediatamente procurar o serviço de emergência.
Na emergência, o paciente deve ser avaliado antes do tratamento broncodilatador inicial-FR, FC, saturação de O2, e iniciar a administração de O2 se estiver indicada. Iniciar então o β2 e fazer nova administração 15-20 min depois (1-2 puffs por inalador dosimetrado [MDI] com espaçador ou nebulização; podendo chegar a 2-4 puffs ou mais, a critério médico e sob monitorização cardiorrespiratória contínua, enquanto for necessária).
Sinais, sintomas e evolução clínica também devem ser monitorados por todo o tempo que o paciente estiver na emergência. Os casos com sinais de piora e progressão da crise durante 4 h de tratamento na sala de emergência devem ser avaliados quanto à necessidade de hospitalização ou encaminhamento à UTI.
Os pacientes com exacerbações agudas de asma devem ser tratados de forma agressiva no setor de emergência. Os pacientes que não melhoram ou aqueles que apresentam piora devem ser hospitalizados ou encaminhados para a unidade de terapia intensiva já que terão um maior monitoramento e escalonamento da terapia.
O tratamento padrão compreende a administração de líquidos, porém não se pode esquecer de que os casos graves fazem síndrome inapropriada de hormônio antidiurético - necessitando de restrição hídrica, instituição imediata de oxigénio, β2 agonistas -MDI ou por nebulização (intermitente ou contínua), devendo-se associar o brometo de ipratrópio de acordo com a gravidade, assim como os corticosteroides. A infusão intravenosa de um agente β2 agonista deve ser feita apenas nos pacientes internados em UTI. A medicação broncodilatadora deve ser iniciada de preferência pela via inalatória, seja com nebulizador e /ou aerossóis dosimetrados com espaçadores. Outras terapias disponíveis na UTI incluem infusões intravenosas de sulfato de magnésio, metilxantina e mistura hélio-oxigênio.
A falta de resposta ao tratamento pode causar deterioração e desenvolvimento de insuficiência respiratória, necessitando o paciente de intubação e suporte ventilatório. Pacientes selecionados na UTI podem beneficiar-se de agentes anestésicos inalatórios, para promover broncodilatação, ou de broncoscopia, para aliviar a obstrução das vias respiratórias por atelectasias resultantes da obstrução brônquica. O tratamento médico agressivo e uma estratégica ventilação mecânica minimizam a hiperinsuflação dinâmica e propiciam baixa morbidade e taxas perto de zero de mortalidade em crianças e adolescentes com asma aguda grave.
Dispositivos para administração de medicamentos por via inalatória
A deposição pulmonar dos medicamentos depende dos tipos de dispositivos inalatórios. A escolha do dispositivo mais adequado depende da análise de vários aspectos, tais como:
1. A satisfação e a adesão ao tratamento podem ser melhoradas se for respeitada, dentro do possível, sua escolha pessoal por determinado dispositivo.
2. A escolha deve ser baseada na otimização do custo/benefício, considerando fatores ligados ao paciente, ao medicamento e aos dispositivos disponíveis no mercado.
3. A maioria dos pacientes quando bem orientados conseguem usar eficientemente os aerossóis dosimetrados.
4. Em pacientes com dificuldade de uso dos aerossóis dosimetrados, inclusive quando acoplados a espaçadores, tem-se como opção os nebulizadores.
5. Nebulizadores de jato são reservados para exacerbações graves em crianças com menos de 3 anos e idosos debilitados ou com dificuldade cognitiva que não conseguem usar corretamente ou não se adaptam aos dispositivos inalatórios.
6. Sempre que possível, usar apenas um tipo de dispositivo para facilitar o aprendizado da técnica e melhorar a adesão ao tratamento.
7. Para reduzir os efeitos adversos, pacientes devem acoplar espaçador ao aerossol dosimetrado e lavar a boca após o uso de dispositivos.
Identificação do asmático de risco
Em quase todos os casos, a causa da morte por asma é a asfixia. Por isso, é preciso identificar os seguintes aspectos, que indicam maior risco para os pacientes:
Crise grave prévia com necessidade de ventilação mecânica ou internação em UTI (constituem os fatores de risco mais fortemente associados a crises fatais ou quase fatais). Três ou mais visitas à emergência ou duas ou mais hospitalizações por asma nos últimos 12 meses. Uso frequente de corticosteroide sistêmico por conta própria. Uso de um ou mais frascos de aerossol dosimetrado de broncodilatador/mês. Problemas psicossociais (ex: depressão dos pais ou do adolescente, baixo nível socioeconômico, dificuldade de acesso à assistência, falta de aderência a tratamentos prévios). Comorbidades - doença cardiovascular ou neurológica. Asma lábil, com marcadas variações de função pulmonar. Má percepção do grau de obstrução brônquica.
Fatores de risco para internação:
Pneumonia associada. História de internação no último ano. Gravidade da doença. Menores de 2 anos ou adolescentes. Imunossupressão primária ou secundária. Comorbidades.
Indicações de internação/hospitalização:
Oximetria < 91% ou ida à emergência nas últimas 24 horas. Hospitalização prévia com admissão em UTI. Hospitalização no último ano. Intubação traqueal há menos de 1 ano. Uso de musculatura acessória. Alteração do estado de consciência. Pulso paradoxal > 10 mmHg em criança e > 18 mmHg em adolescentes.
Recursos terapêuticos utilizados no resgate de sintomas agudos:
Oxigenoterapia
Pacientes com distúrbios ventilatórios severos devido à alteração na V/P apresentam hipoxemia grave. Os pacientes com asma são suscetíveis de apresentar hipoxemia como resultado de shunts intrapulmonares causados por tampão de muco e atelectasia. O tratamento com β2 agonistas também pode contribuir para a hipoxemia, abolindo a vasoconstrição pulmonar regional e aumentando o shunt intrapulmonar. Portanto, o oxigênio umidificado deve ser oferecido como um gás de transporte para nebulizações e /ou continuamente durante o tratamento quando se usa dispositivos MDI com espaçadores. O oxigênio umidificado deve ser administrado a fim de manter uma PaO2 acima de 80 mmHg e saturação de O2 > 91%.
β2 agonistas inalatórios de curta duração
São os medicamentos de escolha para alívio do broncoespasmo durante as exacerbações agudas de asma. Os β2 agonistas são potentes broncodilatadores que devem ser iniciados imediatamente à oxigenoterapia a fim de aliviar a broncoconstrição do músculo liso das vias respiratórias, o principal responsável pela obstrução das vias aéreas.
Podem ser administrados de forma intermitente ou contínua, produzindo broncodilatação em 15 minutos aproximadamente. A administração contínua de β2 agonistas na UTI parece diminuir mais rapidamente a hipercapnia. A dificuldade na obtenção da broncodilatação sustentada após utilização dos β2 agonistas de curta duração indica a necessidade de cursos de corticosteroides orais ou parenteral. Estão disponíveis salbutamol, fenoterol e terbutalina. A via parenteral é uma opção terapêutica nos casos em que não é possível administrar a medicação por via inalatória, quando há fracasso de resposta clínica e antes de se considerar a ventilação assistida no paciente na UTI com asma quase fatal.
Seus principais efeitos adversos são mais acentuados quando administra-se a medicação por via sistêmica: tremores de extremidades, arritmias cardíacas, hipocalemia, acidose láctica e isquemia miocárdica. A administração do β2 agonistas por via inalatória pode ser feita com nebulizador ou com MDI e espaçador. Administram-se a cada15-20 min durante a fase inicial do tratamento, com uma dose de salbutamol o,o5 a o,15mg/kg diluidos em 4 ml de Nacl a 0,9% no nebulizador e (fluxo 6-8 L/min), pode-se utilizar fenoterol ou terbutalina inalada. A dose ótima e a frequência dos β2 agonistas são controversas, porque menos de 1% do medicamento nebulizado é depositado no pulmão. Além disso, o volume corrente, o padrão de respiração e a técnica são os determinantes maiores de entrada do medicamento na via respiratória periférica, porém imprevisíveis em um dado paciente. Após a série inicial de 3 doses de β2 agonistas, a nebulização contínua deve ser iniciada para pacientes que necessitam de tratamento mais frequentemente do que a cada 1 h.
Nos casos de asma quase fatal e de insuficiência respiratória iminente na UTI, a nebulização contínua possibilita rápida melhora clínica e internações mais curtas em comparação com crianças tratadas com o β2 agonistas intermitente. A dose do salbutamol inalatório de forma contínua varia de 0,15 a 0,45 mg /kg/hora-máximo 20 mg/hora.
Na UTI, pode-se fazer o salbutamol venoso (amp. 1 ml/500 mcg) sob supervisão permanente do médico. Preconiza-se uma dose de ataque de 10 mcg/kg em 15 min (na bomba de infusão), seguida de infusão contínua de 0,1-0,2 mcg/kg/min, com aumento de 0,1mcg/kg/min a cada 20 minutos, até o máximo de 3-6 mcg/kg/min.
Uma opção também é a terbutalina (amp. 1 ml/500 mcg), em uma dose de 0,1/kg/min, utilizando-se em média 3 mcg/kg/min. O aumento das taxas de infusão deve ser dinâmico e sob monitorização médica e cardiorespiratória rigorosa.
A dose a ser atingida deve centrar-se na obtenção do desfecho clínico desejado ou no aparecimento de efeitos adversos (frequência cardíaca superior a 180 bpm) e não nos limites máximos de infusão que podem ser atingidos.
Assim que houver melhora da função ventilatória (melhora acentuada do broncoespasmo), o β2 agonista intravenoso deve ser diminuído lentamente para que se reinicie a administração dos broncodilatadores inalatórios.
O critério para reiniciar a via inalatória é a melhora clínica acentuada e, consequentemente, a estabilização nas taxas de infusão da medicação, mantidas por um período mínimo de 4 h. No caso de a criança apresentar melhora importante, a retirada é feita em 24 horas, reduzindo-se a dose até limites mínimos e mantendo a inalação do β2 agonista.
Glicocorticoides orais
Estão indicados no tratamento das exacerbações graves da asma. Devem ser administrados no domicílio a pacientes em tratamento com corticoides inalatórios (CI) durante a exacerbação; no momento da alta dos serviços de emergência, após exacerbação grave. Reduz a inflamação e diminui a produção de muco. Durante a crise aguda grave, prefere-se a via endovenosa, devido ao risco de vômitos e aspiração, mesmo a via oral sendo igualmente eficaz. O início da medicação deve ser feita tão logo esteja indicado, já que sua ação só começa depois de algumas horas após a administração. Os principais efeitos adversos surgem após uso prolongado e/ou administração de doses elevadas, destacando-se entre eles: alterações no metabolismo da glicose, retenção de líquidos, osteoporose, ganho de peso, fácies arredondada, hipertensão arterial e necrose asséptica da cabeça do fêmur.
Medicações de segunda linha Anticolinérgicos inalatórios
O brometo de ipratrópio pode ser usado no tratamento das exacerbações graves de asma, associado ao β2 agonista de curta duração. Entre os efeitos adversos aos anticolinérgicos estão incluídos secura da mucosa oral, glaucoma e retenção urinária. A dose recomendada é de 250 a 500 mcg a cada 6 horas, associada ao β2 agonista. No estado de mal asmático, pode ser feito na primeira hora de permanência na sala de emergência, até de 20 em 20 min.
Sulfato de magnésio
Há evidências de que sulfato de magnésio pode beneficiar adultos e crianças com asma grave. O magnésio é antagonista do cálcio e apresenta relaxamento do músculo liso, provavelmente tem um importante e rápido efeito broncodilatador. O magnésio apresenta alguns efeitos adversos. Dentre eles, o mais comum é a hipotensão. Isso pode ser evitado por meio da infusão da dose ao longo de no mínimo 30 min. Os níveis séricos de 4mg/dl são necessários para se obter o efeito broncodilatador. As diretrizes mais recentes do NIH recomendam a consideração de magnésio para pacientes selecionados. Nesse ponto, a literatura existente indica que o magnésio deve ser considerado para pacientes graves que têm uma resposta subótima a –2, brometo de ipatrópio e corticosteroides, bem como para todas as crianças com crise de asma grave ou quase fatal. Entretanto, há necessidade de monitorização do paciente durante e pós infusão. A dose recomendada é de 25 a 40 mcg/kg/dose com uma infusão de 30 min média.
Teofilina
A metilxantina passou a não ser mais a medicação de escolha após o surgimento do β2 adrenérgico. Todavia, é um broncodilatador que melhora a endurance, amenizando a fadiga dos músculos respiratórios. Deve ser utilizada, portanto, de forma associada evitando efeitos adversos e dosando o nível sérico. Cumpre seu papel nos casos refratários ao β2 e ao esteroide, podendo ser utilizada no paciente na UTI como terapia coadjuvante.
Antibióticos
Só devem ser utilizados quando se comprova infecção bacteriana associada, já que a maioria das vezes o desencadeante é uma infecção viral.
Ventilação mecânica
A utilização da ventilação não invasiva com aplicação de máscara facial é uma opção terapêutica para suporte ventilatório de curto prazo na criança com falência ventilatória hipercapnica, mas ainda em condições de manutenção da via permeável. A ventilação não invasiva com pressão positiva é uma opção atrativa para o tratamento da asma refratária. Na asma aguda grave a utilização de pressão positiva contínua em vias aéreas através de máscara diminui o trabalho respiratório, causa broncodilatação, diminui a resistência de vias aéreas, reexpande áreas de atelectasia, promove a remoção de secreção, permite um repouso dos músculos inspiratórios e do diafragma e diminui os efeitos hemodinâmicos adversos de uma pressão pleural inspiratória muito negativa
A decisão de entubar e ventilar a criança com asma quase fatal ou estado de mal asmático está indicada nos casos de broncoespasmo severo que não responde à terapêutica agressiva iniciada a 60 min, acompanhada de piora da hipoxia e hipercapnia.
Asma quase fatal é identificada por parada respiratória ou evidência de insuficiência respiratória (PaCO2 > 50 mm Hg). Baseia-se em critérios clínicos e gasométricos: fadiga de músculos respiratórios, decréscimo da entrada de ar nos pulmões, deterioração do estado mental, evidenciando piora dos parâmetros gasométricos, hipóxia e hipercarbia. Não esperar parada cardíaca e/ou respiratória e gasping para indicar um procedimento eletivo e que pode ser realizado sob monitorização cardiorrespiratória.
Fatores de risco da ventilação mecânica
Uso de corticoide sistêmico - corticodependência. Ventilação mecânica prévia. Acidose respiratória prévia. Hospitalização nos últimos 12 meses. Entubação e internação em UTI no último ano.
Depois de apropriada sedação, a intubação deve ser feita pelo médico mais experiente e rápido da equipe. A entubação orotraqueal é o método de escolha. A manipulação das vias respiratórias do asmático pode piorar o broncoespasmo ou provocar laringoespasmo. É preciso ter cuidado com manobras de insuflação com ambu que possam provocar hipotensão e pneumotórax. O tubo deve ser temporariamente desconectado para diminuir a pressão das vias respiratórias. O objetivo é reduzir a hiperinsuflação dinâmica, assim o modo ventilatório deve ser empregado visando: diminuição da ventilação / minuto, aumento do tempo expiratório e diminuição da resistência.
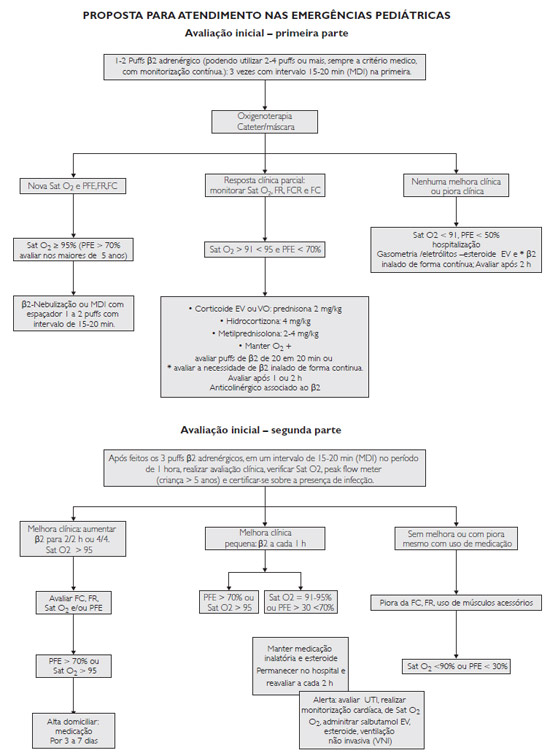
MANEJO DA CRISE AGUDA NA SALA DE EMERGÊNCIA
Medicação de resgate por via inalatória:
Sat O2 > 94-95 %.
O2 sob a forma de máscara ou cateter.
Nebulização com β2 adrenérgico:
Fenoterol ou Salbutamol: 3 nebulizações (uma a cada 15-30 min) com salbutamol gotas ou fenoterol gotas, terbutalina gotas, não ultrapassando 10 gotas. Pode-se também utilizar a fórmula em flaconete do salbutamol para nebulizar-1 a 2 ml de acordo com o pêso da criança ou MDI com espaçador com 1 a 4 puffs de acordo com cada caso, sempre a critério médico e sob monitorização cardiorrespiratória em ambiente hospitalar. Monitorar: frequências respiratória e cardíaca e a saturação de O2.
Se SatO2 > 91 e < 94%: O2 sob a forma de máscara ou cateter, além de β2 adrenérgico, esteroide e anticolinérgico.
No caso de não haver melhora, administrar β2 adrenérgico intermitente de hora em hora ou a cada 2 h ou continuamente e associar anticolinérgico, manter esteroide, além de verificar a presença ou não de infecção bacteriana.
Considerar, após aproximadamente 4 h de medicação, a possibilidade ou não de hospitalização. Monitorar: frequências respiratória e cardíaca e a saturação de O2 Tratar processo infeccioso e complicações, caso estas se apresentem durante ou por ocasião da entrada no serviço de emergência.
Nos casos refratários, com Sat O2 < 90 % e em que o paciente é internado por não resposta à terapêutica anteriormente realizada:
Considerar UTI:
As medicações a seguir devem ser administradas com acompanhamento do intensivista:
Salbutamol endovenoso na UTI: considerar β2 agonista (na bomba de infusão) na dose de 10 µg/kg imediata por 10 a 15 minutos, depois iniciar infusão contínua de 0,1-0,2 µg/kg/min, podendo-se aumentar a velocidade de infusão para 0,1 µg/kg/min, não devendo ultrapassar 3-6 µg/kg/min. Atenção para arritmias: monitorização contínua, diminuição velocidade de infusão caso ocorra taquicardia (180 bpm). Monitorar CK, CKMB. Esteroide parenteral: hidrocortizona 2-4 mg/kg/dose a cada 6 horas. A dose não pode ultrapassar 20 mg/kg/dia ou metilprednisolona 2 mg/kg/dia de ataque e manter com 0,5 a 1 mg /kg /dose a cada 6 horas. Aminofilina venosa (na bomba de infusão contínua): crianças 0,4-0,8 mg/kg/h (1 a 9 anos) podendo chegar a 1 mg/kg/h ou 0,6 mg/kg/h (acima de 9 anos). Verificar se houve uso prévio de xantina e monitorar níveis séricos. Sulfato de magnésio: 2,5 mg/kg/min diluídos em solução fisiológica, durante 30 min ou mais, lentamente; dose total de 50 mg/kg, até um máximo de 2 g, no gotejo de 1 ml/kg/hora. Prestar atenção aos efeitos adversos, como hipotensão grave. Mistura de hélio e oxigênio: o hélio possui uma densidade 3 vezes menor que a do ar ambiente ou do oxigênio puro. A baixa densidade do gás pode transformar um fluxo aéreo turbulento em um fluxo laminar e, consequentemente, proporcionar redução da resistência nas vias respiratórias, resultando em diminuição da pressão inspiratória e do trabalho respiratório. Além disso, o hélio aumenta a difusão do gás carbônico e pode melhorar a ventilação alveolar. São essas as propriedades que tornam essa mistura uma alternativa a ser considerada no tratamento de pacientes com asma e outros quadros de obstrução respiratória grave. A mistura é feita com 70% de helio e 20 de oxigênio.
A Ketamina é uma opção terapêutica no caso de não resposta dos pacientes em UTI.
Broncoscopia
Deve ser considerada nos pacientes graves, refratária a medicação, para pacientes com tampão mucoso e secreção espessa, com ou sem atelectasia associada.
Circulação extracorpórea
É utilizada para pacientes graves com nenhuma resposta à terapêutica e com instabilidade clínica e máximas doses de medicamentos. Tem sido ainda pouca utilizada em crianças.
CONCLUSÃO
Ao oxigenoterapia é a primeira medida a ser tomada diante de um paciente com asma aguda na sala de emergência. O inalador dosimetrado acoplado ao espaçador é o dispositivo de escolha para se administrar medicação na sala de emergência. A medicação de resgate e o esteroide, oral ou parenteral, resolvem a maioria de casos de asma aguda. FC, FR, Sat O2 e a classificação de gravidade determinam o tratamento e o acompanhamento. Diante de piora clínica, da Sat O2 < 91%, FC, FR e dos parâmetros funcionais deve-se considerar hospitalização. Se não houver melhora em 4 h de tratamento na sala de emergência, avaliar inclusive se há indicação de terapia intensiva.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Bacharier LB, Boner A, Carlsen KH et al. European Pediatric Asthma Group. Diagnosis and treatment of asthma in childhood: a PRACTALL consensus report. Allergy. 2008 Jan;63(1):5-34.
2. Biarent D. Therapeutic strategies in near fatal asthma in children. Pediatric Pulmonology. 2001;23:90-93.
3. British Thoracic Society. Scottish Intercollegiate Network. British Guidelines on the management of Asthma.Thorax, 2008.
4. Consenso Brasileiro de Asma. Jornal Brasileiro de Pneumologia. Abril 2012 (no prelo).
5. Carroll LC, Schramm MC, Zucker RA. Slow responders to IV - 2 adrenergic agonist therapy. Pediatric Pulmonology. 2008;43:627-33.
6. Indicadores e Dados Básicos 2008: tabnet.datasus.gov.br/cgi/idb2008.
7. Expert Panel Report 3: guidelines for the diagnosis and management of asthma. 2007;1-440.
8. Fulbrigge A, Peden D, Apter AJ,Boushey H.A;Camargo C.A; Gern J;Heymann P.W;Martinez F.D;Mauger D;Teague W.G;Blaisdell C et al. Asthma outcomes: exacerbations. J Allergy Clin Immunol. 2012;129:S34-48.
9. GINA. Global strategy for asthma management and prevention. Global Iniciative Asthma 2010 (cited 2011 April).Disponível em: http://www.ginasthma.org.
10. Muchão PF, Ferreira da Silva LV. Advances in inhalation therapy in pediatrics. J Pediatr. 2010;367-76.
11. Levy LM, Thomas RI, Pearce L et al. Summary of the 2008 BTS/SIGN British guideline on the management of asthma. Primary Care Respiratory Journal. 2009;18:S1-S16.
12. Platts-Mills T,Adachi M, Busse WW et al. Allergy. 4. ed. Elsevier. 2012;181-202,432.
13. Alexandre T, Rotta, Veda L Ackerman, Howard Eigen Asthma in: Bradley Fuhrman and Jerry Zimmerman Pediatric Critical care 4 edition, 2011;575-589. MOSBI.
AVALIAÇÃO
36. Sobre a crise aguda de asma, assinale apenas as verdadeiras:
a) Oxigenoterapia - manter Sat O2 > 94%.
b) O β2 de alívio e o O2 devem ser iniciados imediatamente na sala de emergência.
c) O esteroide parenteral deve ser administrado assim que o paciente chega ao hospital.
d) Oxigenoterapia deve ser iniciada apenas após o tratamento com o β2 de alívio.
Qual alternativa é correta?
a) Verdadeiras apenas as letras A,B,C.
b) Todas são verdadeiras.
c) Somente a letra C é verdadeira.
d) Somente as letras A e B são verdadeiras.
e) Nenhuma letra é verdadeira.
37. Os fatores de risco para internação são:
a) Oximetria < 91% ou ida à Emergência nas últimas 24 h.
b) Hospitalização prévia com admissão em UTI.
c) Oximetria entre 91 e 94%, sem internação prévia.
d) Alteração do estado de consciência.
e) Pulso paradoxal >10 mmHg em criança e >18 mmHg em adolescentes.
Considera(m)-se incorretas:
a) Letras A e B.
b) Todas estão incorretas.
c) Letras A e C.
d) Letra B apenas.
e) Apenas letra C.
38. Entre as alternativas a seguir, qual a primeira conduta na sala de emergência?
a) β2 adrenérgico via oral.
b) β2 adrenérgico via inalatória.
c) Oxigenoterapia.
d) Nebulização com β2 adrenérgico.
e) Nebulização com β2 adrenérgico e anticolinérgico.
39.O esteroide deve ser utilizado:
a) Imediatamente ao chegar à Emergência.
b) Apenas pela via parenteral.
c) Somente pela via inalatória.
d) Pode ser utilizado pela via oral.
e) Associado ao anticolinérgico.
40. De acordo com a classificação de gravidade, consideramos o quadro severo quando:
a) FC > 100.
b) Sat O2 < 95%.
c) Pa CO2 > 45.
d) Pa O2 até 60.
e) FR > 50.
41. Entre os efeitos adversos do β2, podemos citar:
a) Hipercalemia, acidose láctica e taquicardia.
b) Hipocalemia, alcalose metabólica, bradicardia.
c) Tremores de extremidades, arritmia cardíaca, hipercalemia.
d) Hipocalemia, acidose láctica, isquemia cardíaca.
e) Hipercalemia, hipercapnia, acidose láctica.
Qual a alternativa correta?
a) Somente A.
b) A,C,D.
c) Somente D.
d) Somente C e D.
e) Somente B.